题目内容
为了测定某纯碱样品中碳酸钠的质量分数,取该样品与足量稀盐酸在烧杯中反应,有关实验数据如下表。
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 纯碱样品的质量/g | 烧杯和其中混合物的质量/g |
| 120 | 12 | 127.6 |
请计算:(1)该反应生成二氧化碳的质量为 g。
(2)该纯碱样品中碳酸钠的质量分数为多少。(请写出计算过程)
(1)4.4  (1分)
(1分)
(2)设样品中碳酸钠的质量为x
2HCl + Na2CO3 2NaCl + H2O + CO2 ↑
 106 44
106 44
x 4.4 g
106/44 = x/4.4
X = 10.6 g (2分)
样品中碳酸钠的质量分数是
10.6 g/12 g × 100% = 88.3% (2分)

下列不可直接加热的仪器是( )
|
| A. | 烧杯 | B. | 试管 | C. | 蒸发皿 | D. | 燃烧匙 |
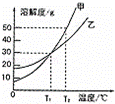
甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是( )
|
| A. | T2℃时甲和乙的饱和溶液,降到T1℃时,甲乙仍是饱和溶液且有晶体析出 |
|
| B. | 甲和乙的溶解度相等 |
|
| C. | T1℃时,甲和乙各30g分别加入100g水中,均形成饱和溶液 |
|
| D. | T2℃时,100g甲的饱和溶液里含有溶质甲的质量为50g |
如图是某品牌牙膏包装盒上的部分说明,这里的碳酸钙和水都属于( )
|
| A. | 盐 | B. | 氧化物 | C. | 单质 | D. | 化合物 |
 ; (2)常用作燃料 ;
; (2)常用作燃料 ;