题目内容
17.我国首台使用二甲醚为燃料的城市客车有效地解决了公交车冒黑烟的问题.已知二甲醚的化学式为C2H6O,计算:
(1)二甲醚的相对分子质量是46,其中碳、氢元素的质量比为4:1.
(2)132g的二甲醚与多少克的二氧化碳所含碳元素的质量相等?
分析 (1)根据相对分子质量为构成分子的各原子的相对原子质量之和,化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)二甲醚的相对分子质量是12×2+1×6+16=46.
其中碳、氢元素的质量比为(12×2):(1×6)=4:1.
(2)设需要二氧化碳的质量为x
132g×$\frac{12×2}{46}×$100%=x×$\frac{12}{12+16×2}×$100% x≈252.5g.
故答案为:(1)46;4:1;(2)与252.5g的二氧化碳所含碳元素的质量相等.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
7. 将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示:已知:A、B、C在生成物中均为+2价,根据图中所提供的信息,得出的结论正确的是( )
将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示:已知:A、B、C在生成物中均为+2价,根据图中所提供的信息,得出的结论正确的是( )
 将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示:已知:A、B、C在生成物中均为+2价,根据图中所提供的信息,得出的结论正确的是( )
将质量相等的A、B、C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示:已知:A、B、C在生成物中均为+2价,根据图中所提供的信息,得出的结论正确的是( )| A. | 放出H2的质量是B>A>C | B. | 金属活动性顺序是A>B>C | ||
| C. | 反应速率大小顺序是A>B>C | D. | 相对原子质量大小顺序是C>B>A |
12.同学们应用数字化实验探究外界条件对双氧水分解速率的影响.实验装置如图:
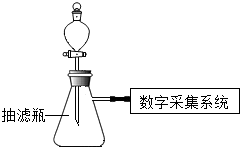
【进行实验】
【解释与结论】
(1)实验1的2号抽滤瓶中反应的化学方程式为2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)某同学得到“不同催化剂的催化效果不同”的结论,他的依据是实验1中2、3号瓶曲线不同.
(3)通过上述实验得到:影响该反应速率的外界因素有催化剂种类、反应物浓度、温度.
【反思与评价】
(4)经过多次实验,有的同学对比实验1的3号瓶、实验2的2号瓶中同为40s时的气体压强,发现存在较大的差异,可能的原因是实验温度不同.

【进行实验】
| 序号 | 主要实验步骤 | 装置内压强-时间图象 |
| 实 验 1 | ①1号抽滤瓶中不加任何试剂, 2号抽滤瓶中加入0.2gMnO2粉末, 3号抽滤瓶中加入0.2gFeCl3粉末. ②用三支分液漏斗分别加入15mL4%的H2O2溶液. | 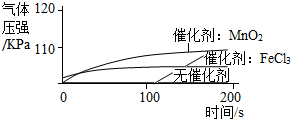 |
| 实 验 2 | ①三个抽滤瓶中分别加入0.2g FeCl3粉末. ②分别用1号分液漏斗加入15mL2%的H2O2溶液;用2号分液漏斗加入15mL4%的H2O2溶液;用3号分液漏斗加入15mL6%的H2O2溶液. | 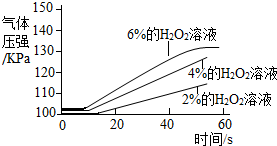 |
| 实 验 3 | ①三个抽滤瓶中分别加入0.2g FeCl3粉末,分别放入装有10℃、20℃、40℃水的水槽中. ②用三支分液漏斗分别加入15mL4%的H2O2溶液. |  |
(1)实验1的2号抽滤瓶中反应的化学方程式为2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)某同学得到“不同催化剂的催化效果不同”的结论,他的依据是实验1中2、3号瓶曲线不同.
(3)通过上述实验得到:影响该反应速率的外界因素有催化剂种类、反应物浓度、温度.
【反思与评价】
(4)经过多次实验,有的同学对比实验1的3号瓶、实验2的2号瓶中同为40s时的气体压强,发现存在较大的差异,可能的原因是实验温度不同.
9.碳12原子的质量为1.993×1026kg,一种M原子的质量为9.288×10-26kg,则M原子的相对原子质量约是( )
| A. | 24 | B. | 27 | C. | 56 | D. | 108 |
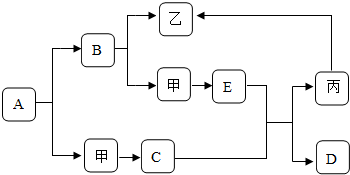 右图是初中化学中常见物质间的转化关系,其中甲、乙、丙为单质;A、B、C、D、E为化合物,且A与B的组成元素相同,D与E的组成元素也相同.已知C、丙均为黑色粉末,C和E在一定条件下可生成丙和D,D能使澄清的石灰水变浑浊.其余反应条件、部分反应物和生成物均已略去.试推断:
右图是初中化学中常见物质间的转化关系,其中甲、乙、丙为单质;A、B、C、D、E为化合物,且A与B的组成元素相同,D与E的组成元素也相同.已知C、丙均为黑色粉末,C和E在一定条件下可生成丙和D,D能使澄清的石灰水变浑浊.其余反应条件、部分反应物和生成物均已略去.试推断: