题目内容
1.使用尿素处理尾气可使重型柴油车达到国IV排放标准.其原理是尿素[CO(NH2)2]与汽车尾气中的氮氧化物(如二氧化氮)反应,生成无污染的气体排出.(1)尿素属于氮肥.
(2)尿素中碳氢元素质量比:3:1.
(3)补全尿素与二氧化氮反应的化学方程式:4CO(NH2)2+6NO2$\frac{\underline{\;一定条件\;}}{\;}$4CO2+8H2O+7N2.
分析 (1)含有氮元素的肥料称为氮肥;
(2)根据元素质量比进行分析解答.
(3)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
解答 解:(1)尿素含有氮元素,为氮肥;
(2)尿素中碳氢元素质量比12:4=3:1;
(3)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式,反应前碳、氢、氧、氮原子个数分别为4、16、16、14,反应后的生成物中碳、氢、氧、氮原子个数分别为4、16、16、0,根据反应前后原子种类、数目不变,则生成物的分子中含有14个氮原子,则横线上应填的是7N2.
故答案为:(1)氮 (2)3:1 (3)7N2
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
11.永嘉东藁的“柿子”已经享誉全省.今年来某果农发现其种植的柿子出现生长迟缓、叶色淡黄的现象,经农技员诊断必须追加相应的复合肥料,你认为应选用( )
| A. | CO(NH2)2 | B. | NH4Cl | C. | K2SO4 | D. | (NH4)2HPO4 |
12.某农场有一袋标签已脱落的化肥,只知道它是NH4Cl、(NH4)2SO4、NH4HCO3中的一种.请通过一下实验确定它是哪种化肥?
| 实验步骤 | 实验现象及结论 |
| (1)取少量的样品于试管中,滴入适量的稀盐酸 | 若没有气泡产生,则该化肥一定不是 NH4HCO3 |
| (2)在步骤(1)的试管中再滴入足量氯化钡溶液溶液 | 若无白色沉淀产生,则该化肥是NH4Cl 若有白色沉淀产生,则该化肥是 (NH4)2SO4 |
9.下列除去杂质的方法正确的是( )
| 选项 | 物质 | 所含杂质 | 除杂质的试剂及操作 |
| A | CO2 | HCl | 通入足量的NaOH溶液,干燥 |
| B | CaO | CaCO3 | 加入适量的稀盐酸,蒸发 |
| C | KCl溶液 | K2SO4 | 加入过量的BaCl2溶液、过滤 |
| D | NaCl溶液 | MgCl2 | 加入适量的NaOH溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
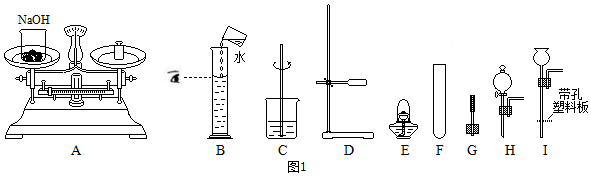
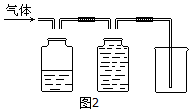
6.下列图示实验基本操作正确的是( )
| A. | 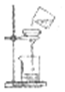 | B. |  | C. |  | D. | 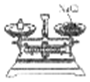 |
13.第30届伦敦夏季奥运会将于2012年7月27日晚20时12分(伦敦当地时间)开幕.从安全角度考虑,以下四种物质中,允许旅客带上地铁的是( )
| A. | 浓硫酸 | B. | 食盐 | C. | 固体氢氧化钠 | D. | 白磷 |
10.蒸馒头时,面碱(主要含Na2CO3 )放多了会发黄,为了除去过多的面碱,做馒头时可加入适量的( )
| A. | 食盐 | B. | 食醋 | C. | 黄酒 | D. | 白糖 |