题目内容
按要求填写
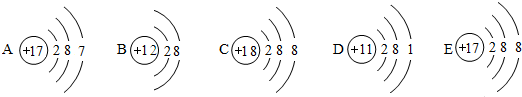
如图是五种粒子的结构示意图,图中粒子共能表示 种元素,图中表示的稀有气体原子是 (用原子符号表示),表示的阳离子是 (用离子符号表示),表示的阴离子是 (用离子符号表示),二者形成的化合物的化学式为 .

如图是五种粒子的结构示意图,图中粒子共能表示
考点:原子结构示意图与离子结构示意图,化学符号及其周围数字的意义
专题:化学用语和质量守恒定律
分析:根据不同种元素最本质的区别是质子数不同,进行分析解答;若原子的最外层电子数为8,则为稀有气体元素,属于相对稳定结构;根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;据此进行分析解答.
解答:解:根据不同种元素最本质的区别是质子数不同,图中粒子的核内质子数分别为17、12、18、11,共表示4种元素.C质子数=核外电子数=18,为原子,且最外层电子数为8,则为稀有气体元素;B质子数=12,核外电子数=10,质子数>核外电子数,为阳离子,其离子符号为Mg2+;E质子数=17,核外电子数=18,质子数<核外电子数,为阴离子,其离子符号为Cl-;二者形成的化合物为氯化镁,其化学式为MgCl2.
故答案为:4;C;Mg2+;Cl-;MgCl2.
故答案为:4;C;Mg2+;Cl-;MgCl2.
点评:本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.

练习册系列答案
相关题目
下列化学方程式符合题意且书写正确的是( )
| A、证明锌的活动性比铁强:3Zn+2FeCl3=2Fe+3ZnCl2↑ | ||||
| B、医疗上用氢氧化镁中和过多胃酸:Mg(OH)2+2HCl=MgCl2+H2O | ||||
C、工业上用高温煅烧石灰石的方法制生石灰:CaCO3
| ||||
| D、正常雨水的pH小于7的原因:CO2+H2O=H2CO3 |
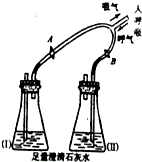 人体通过肺与外界进行气体交换,吸入空气中的氧气,排出二氧化碳和水蒸气.但人体排出的二氧化碳究竟是空气中原有的,还是人体代谢的最终产物?为了证实这个问题,有人采用了如图所示装置进行实验.
人体通过肺与外界进行气体交换,吸入空气中的氧气,排出二氧化碳和水蒸气.但人体排出的二氧化碳究竟是空气中原有的,还是人体代谢的最终产物?为了证实这个问题,有人采用了如图所示装置进行实验.
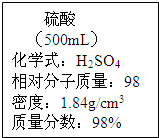 实验室一瓶浓硫酸的商标如图所示,根据有关信息计算.
实验室一瓶浓硫酸的商标如图所示,根据有关信息计算.