��Ŀ����
11��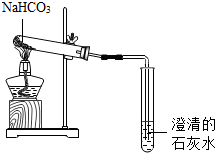 Na2CO3��NaHCO3�������г������Σ�ijʵ��С��ͨ������ʵ�����о����������ʵ����ʣ���֪��Na2CO3��NaHCO3��ˮ��Һ�ʼ��ԣ�NaHCO3�����ֽ�����Na2CO3��H2O��CO2����
Na2CO3��NaHCO3�������г������Σ�ijʵ��С��ͨ������ʵ�����о����������ʵ����ʣ���֪��Na2CO3��NaHCO3��ˮ��Һ�ʼ��ԣ�NaHCO3�����ֽ�����Na2CO3��H2O��CO2������1����ȡ���ֹ����1g�ֱ������֧�Թ��У��ټ���5mLˮ�����������ܽ⣬���ָ������£�
�ٷ���Na2CO3��ȫ�ܽ⣬��NaHCO3��ʣ�࣮�ɴ˵ó����ۣ�����ͬ�¶��£�ͬ���������ֹ�����ͬ������ܼ��У�Na2CO3��NaHCO3������ˮ��
����������Һ�и�����1��2�η�̪��Һ����Һ���ʺ�ɫ��
��2����ȡ����NaHCO3����ͼװ�ý���ʵ�飬�ɹ۲���������ǣ����Թܿ���ˮ�����ɣ�����ʯ��ˮ����ǣ�
���ü��ȵķ�����ȥ����Na2CO3��ĩ��������NaHCO3��
��3���ⶨNa2CO3��Ʒ����NaCl���ʣ���Na2CO3������������
�ٳ�ȡmg��Ʒ�����ձ��м�ˮ�ܽ⣻
�ڼ��������CaCl2��Һ��ַ�Ӧ����Ӧ�Ļ�ѧ����ʽΪNa2CO3+CaCl2=CaCO3��+2NaCl��֤����Ӧ��CaCl2��ʣ��ķ������ټ���̼���ƣ��а�ɫ�������ɣ�
�۹��ˡ�ϴ�ӡ���������ⶨ������Ϊng������Ʒ��Na2CO3����������Ϊ$\frac{106n}{m}$%��
���� ��1���ٳ����£�ͬ������ͬ������ܼ���Na2CO3������ȫ�ܽ⣬��NaHCO3������ʣ�࣬˵��Na2CO3��NaHCO3���ܣ�
��̼���ƺ�̼�����Ƶ���Һ�Լ��Խ��
��2������̼�������ȶ��Բ�����ֽ⣬���ɶ�����̼���壬������̼���������Ʒ�Ӧ����̼��Ƴ������
��3������̼���ƺ��Ȼ��Ʒ�Ӧ����̼��Ƴ������Ȼ��ƽ�����÷�Ӧ�ķ���ʽ������������Ϊ̼��Ƶ����������̼���Ƶ��������
��� �⣺��1���ٳ�ȡ���ֹ����1g���ֱ��������С�ձ��У��ٸ��μ�5mL����ˮ���������¶ȱ仯�����������ܽ⣬���ָ������º���Na2CO3������ȫ�ܽ⣬��NaHCO3������ʣ�࣬˵����ͬ�����¶��£�ͬ���������ֹ�����ͬ������ܼ��У�Na2CO3��NaHCO3������ˮ��
��̼���ƺ�̼�����Ƶ���Һ�Լ��ԣ���������Һ�и�����1��2�η�̪��Һ����Һ���ʺ�ɫ��
��2����̼�����������ֽ⣬2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+CO2��+H2O���ɹ۲���������ǣ����Թܿ���ˮ�����ɣ����ɵ�CO2����ͨ�����ʯ��ˮ������ʯ��ˮ����ǣ�
��̼���Ƽ��Ȳ��ֽ⣬̼�����������ֽ⣬�ü��ȵķ�����ȥ����Na2CO3��ĩ��������NaHCO3��
��3����̼���ƺ��Ȼ��Ʒ�Ӧ����̼��Ƴ������Ȼ��ƣ���ѧ���̷���ʽΪ��Na2CO3+CaCl2=CaCO3��+2NaCl��֤����Ӧ��CaCl2��ʣ��ķ������ټ���̼���ƣ��а�ɫ�������ɣ�
����̼������Ʒ��̼���Ƶ�����Ϊx��
Na2CO3+CaCl2=CaCO3��+2NaCl
106 100
x ng
$\frac{106}{x}=\frac{100}{ng}$
x=$\frac{106n}{100}g$
��Ʒ��Na2CO3����������Ϊ$\frac{\frac{106n}{100}g}{mg}��$100%=$\frac{53n}{50m}$��100%=$\frac{106n}{m}$%
�𰸣�
��1����ͬ���������ֹ�����ͬ������ܼ��У�Na2CO3��NaHCO3������ˮ���ں죻
��2���ٳ���ʯ��ˮ����ǣ��ڼ��ȣ�
��3����Na2CO3+CaCl2=CaCO3��+2NaCl �ټ���̼���ƣ��а�ɫ�������ɣ�
��$\frac{106n}{m}$%��
���� ���⿼��Na2CO3��NaHCO3���ʵıȽϣ���Ŀ�Ѷ��еȣ�ע�����Na2CO3��NaHCO3�����Լ���ط�Ӧ�ķ���ʽ����д��

 ��ʦ�㲦��ϵ�д�
��ʦ�㲦��ϵ�д� Ӣ�żƻ���ĩ����ϵ�д�
Ӣ�żƻ���ĩ����ϵ�д�| A�� | ��˿�ڿ����о���ȼ�գ��������䣬���ɺ�ɫ���� | |
| B�� | ��ȼһ������ά�������ս���ë����ζ | |
| C�� | ͭƬͶ�뵽ϡ�����в������������� | |
| D�� | �ò�������ϡ����ε�pH��ֽ�ϣ���ֽ�ɻ�ɫ��Ϊ��ɫ |
| ϡ�������� | ��1�� | ��2�� | ��3�� | ��4�� | ��5�� | ��6�� |
| ʣ��������� | 2.4g | m | n | 0.6g | 0.6g | 0.6g |
��2���Ͻ���Ʒ��þ������������80%
��2����ʽ��������ϡ������H2SO4������������
| A�� |  �μ�Һ�� | B�� |  �������� | C�� |  ������Һ��pH | D�� |  ���װ�������� |
| A�� | -2 | B�� | +2 | C�� | +4 | D�� | +6 |
| A�� | ����������ȼ�գ��ᷢ������������ɫ���棬�����д̼�����ζ������ | |
| B�� | ϸ��˿�������е�ȼʱ������ȼ�գ��������䣬���ɺ�ɫ���� | |
| C�� | ��ȼһ����̼ʱ���������ɫ��������ʹ����ʯ��ˮ����� | |
| D�� | �ڿ����д�ʢŨ������Լ�ƿƿ�����д̼�����ζ���������� |
| A�� | ������˽�ҳ����� | B�� | ����ʹ��̫������ˮ�� | ||
| C�� | ������ú�������� | D�� | ����¶��������� |
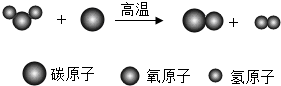 ��ͼΪij��Ӧ����ģ��ʾ��ͼ��
��ͼΪij��Ӧ����ģ��ʾ��ͼ��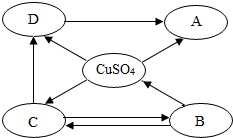 ����֪ʶ������ѧϰ��ѧ����Ҫ��������ͼ�Dz�ͬ�����ת����ϵͼ������A��B��C��D���ڲ�ͬ�������ʣ��Ҷ�����ͭԪ�أ�BΪ��ɫ��ĩ��CΪ��ɫ��ĩ����������ʾһ������һ��ת������һ�����ʣ����ַ�Ӧ������P��Ӧ����δ���������ش����⣺
����֪ʶ������ѧϰ��ѧ����Ҫ��������ͼ�Dz�ͬ�����ת����ϵͼ������A��B��C��D���ڲ�ͬ�������ʣ��Ҷ�����ͭԪ�أ�BΪ��ɫ��ĩ��CΪ��ɫ��ĩ����������ʾһ������һ��ת������һ�����ʣ����ַ�Ӧ������P��Ӧ����δ���������ش����⣺