题目内容
14.用玻璃管向盛有紫色石蕊试液的试管中吹气,过一会儿再给试管加热.据此回答:(1)试管中颜色的变化:由紫→红→紫.
(2)写出变化的文字表达式及所属的基本反应类型.
①CO2+H2O=H2CO3,属于化合反应.
②H2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑,属于分解反应.
分析 根据二氧化碳可以与水反应生成碳酸,碳酸能使石蕊变红,碳酸不稳定,受热易分解分析.
解答 解:二氧化碳可以与水反应生成碳酸,碳酸显酸性,能使石蕊变红,碳酸不稳定,受热易分解为二氧化碳和水,酸性消失,两个反应分别是“多变一”的化合反应和“一变多”的分解反应;所以本题答案为:(1)紫,红,紫;(2)CO2+H2O=H2CO3,化合,H2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑,分解.
点评 本题考查了二氧化碳的有关性质,完成此题,可以依据已有的知识进行分析,难度不大.

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
7.科学家培育出一种”食电“细菌,它吃进电能,把二氧化碳和水转化为甲烷等物质,下列说法中不正确的是( )
| A. | 甲烷是组成最简单的有机物 | |
| B. | 细菌“食电”过程可能会释放出氧气 | |
| C. | 这种方法能缓解白色污染 | |
| D. | 通过化学变化可以实现物质及能量的转化 |
8.${\;}_{8}^{16}$O表示该氧元素的原子有8个质子,8个中子.现有两个容器分别充满${\;}_{7}^{14}$N、${\;}_{6}^{13}$C、${\;}_{8}^{16}$O三种原子构成的一氧化氮(NO)和一氧化碳(CO)(两个容器中分别含有相同的分子数).下列说法正确的是( )
| A. | 所含物质的质量和质子数相等 | B. | 含有相同数目的中子和原子 | ||
| C. | 含有相同数目的质子和中子 | D. | 含有相同数目的电子和中子 |
9.下列物质中,既能与Ca(OH)2溶液反应,又能与稀盐酸反应的是( )
| A. | KNO3 | B. | FeCl 3 | C. | Na2CO3 | D. | Fe2O3 |
19.下列四种说法正确的有( )
| A. | 一般不用点燃的方法除去CO2中少量的CO | |
| B. | 1g金属a和1g金属b分别与足量酸充分反应,产生氢气的质量比等于b和a的相对原子质量之比 | |
| C. | 一定质量的某有机物充分燃烧,消耗48g氧气,生成44g二氧化碳和27g水,说明该有机物的组成中含氧元素 | |
| D. | 煤炉越扇越旺,蜡烛一扇就灭,是因为扇蜡烛会降低石蜡着火点 |
6.在实验探究课上,老师给同学们一包红色粉末,该粉末是铜粉和氧化铁粉末(Fe2O3)中的一种或两种.同学们为确定该粉末的成分,进行如下探究.请回答下列问题.
[查阅资料]金属氧化物能够溶于稀硫酸,形成黄色溶液;铜不溶于稀硫酸;铁粉为黑色粉粉末
[提出问题]红色粉末成分是什么?
[猜想假设]猜想1:红色粉末是铜粉(填物质名称);猜想2:红色粉末是氧化铁;猜想3:红色粉末是铜和氧化铁(填物质名称)的混合物.
[设计方案]取少量红色粉末放入硬质玻璃管中,A(填字母序号),充分反应并观察现象(实验装置如图所示).
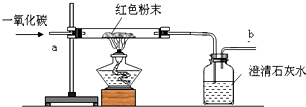
A.先通入一段时间的一氧化碳,然后再点燃酒精灯加热
B.先点燃酒精灯加热一段时间,然后再通入一氧化碳 请你完成下表:
[实验结论]同学们进行了实验并经过分析,确认猜想3成立.
[反思评价]请你用另一种反应原理证明猜想3成立,实验方案是取少量红色粉末于试管中,加入足量的稀盐酸充分反应,试管底部有红色固体剩余,溶液变为黄色,则猜想3成立.此实验从环保角度讲缺少.
[查阅资料]金属氧化物能够溶于稀硫酸,形成黄色溶液;铜不溶于稀硫酸;铁粉为黑色粉粉末
[提出问题]红色粉末成分是什么?
[猜想假设]猜想1:红色粉末是铜粉(填物质名称);猜想2:红色粉末是氧化铁;猜想3:红色粉末是铜和氧化铁(填物质名称)的混合物.
[设计方案]取少量红色粉末放入硬质玻璃管中,A(填字母序号),充分反应并观察现象(实验装置如图所示).

A.先通入一段时间的一氧化碳,然后再点燃酒精灯加热
B.先点燃酒精灯加热一段时间,然后再通入一氧化碳 请你完成下表:
| 实验中可能出现的现象 | 结论 |
| 现象1:红色粉末不变色 | 猜想①1成立 |
| 现象2:红色粉末全部变为②黑色,石灰水变浑浊 | 猜想③2成立 |
| 现象2:红色粉末部分变为④黑色,石灰水变浑浊 | 猜想⑤3成立 |
[反思评价]请你用另一种反应原理证明猜想3成立,实验方案是取少量红色粉末于试管中,加入足量的稀盐酸充分反应,试管底部有红色固体剩余,溶液变为黄色,则猜想3成立.此实验从环保角度讲缺少.
 有如图的仪器
有如图的仪器