题目内容
19.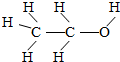 农作物的种子经过发酵、蒸馏制得的乙醇被称为“绿色汽油”.乙醇的分子结构如图所示,则下列叙述正确的是( )
农作物的种子经过发酵、蒸馏制得的乙醇被称为“绿色汽油”.乙醇的分子结构如图所示,则下列叙述正确的是( )| A. | 乙醇是由碳、氢、氧原子构成的有机化合物 | |
| B. | 乙醇分子中碳、氢原子的个数比为1:3 | |
| C. | 乙醇分子中碳、氧元素的质量比为3:2 | |
| D. | 乙醇分子中含2个碳原子、6个氢原子和1个氧原子 |
分析 A.根据物质的结构来分析;
B.根据分子结构来分析;
C.根据分子结构来分析;
D.根据分子结构来分析.
解答 解:由分子结构模型可知,乙醇的化学式为C2H6O.
A.乙醇不是由原子直接构成的,而是由乙醇分子构成的,故错误;
B.一个乙醇分子由2个碳原子、6个氢原子和一个氧原子构成,碳、氢原子的个数比为1:3,故正确;
C.分子中含有的是原子而不是元素,故错误;
D.一个乙醇分子由2个碳原子、6个氢原子和一个氧原子构成,故错误.
故选B.
点评 本题考查化学式的意义以及化学式的简单计算,综合性较强,进一步考查原子的构成,属于简单的信息给予题型,通过结构式获得所需的信息.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
1.下列实验操作正确的是( )
| A. |  取少量液体 | B. |  加入块状固体 | C. |  点燃酒精灯 | D. |  检査装置气密性 |
7. a、b两种物质的溶解度曲线如图所示.下列说法正确的是( )
a、b两种物质的溶解度曲线如图所示.下列说法正确的是( )
 a、b两种物质的溶解度曲线如图所示.下列说法正确的是( )
a、b两种物质的溶解度曲线如图所示.下列说法正确的是( )| A. | 15℃时,a、b的饱和溶液溶质质量分数相等 | |
| B. | 加水或升温均可使a、b的饱和溶液变为不饱和溶液 | |
| C. | 将15℃时b的饱和溶液升温至30℃,溶质质量分数变大 | |
| D. | 15℃时分别向100 g水中加入20 g a和b,降温至0℃,所得溶液均为饱和溶液 |
4.下列关于电解水实验(如图)的叙述正确的是( )


| A. | 甲试管内产生的气体不能使带火星的木条复燃 | |
| B. | 甲、乙两试管产生的气体质量之比为1:2 | |
| C. | 该反应为化合反应 | |
| D. | 实验说明水是由氢元素和氧元素组成的 |
11.下列各项措施中,属于乳化在日常生产生活中的应用的是( )
| A. | 用热的纯碱洗去餐具上的油污 | |
| B. | 用肥皂洗去衣服上的油渍 | |
| C. | 用汽油洗去机修工手上的油污 | |
| D. | 用盐酸清洗盛石灰水试剂瓶瓶壁上的“白膜”(碳酸钙) |

 超市中接触到下列用品.
超市中接触到下列用品. 2012年6月24日,中国载人航天工程实现新突破,神舟九号航天员成功驾驶飞船与天宫一号目标飞行器对接,这标志着中国成为世界上第三个完整掌握空间交会对接技术的国家.
2012年6月24日,中国载人航天工程实现新突破,神舟九号航天员成功驾驶飞船与天宫一号目标飞行器对接,这标志着中国成为世界上第三个完整掌握空间交会对接技术的国家.