题目内容
18.量取47毫升的水,应选用下列( )| A. | 100毫升的量筒 | B. | 100毫升的量筒和滴管 | ||
| C. | 50毫升的量筒和滴管 | D. | 50毫升的量筒 |
分析 量筒量程选择的依据有两点:一是保证测量一次,二是量程要与液体的取用量最接近;据此进行分析解答.
解答 解:量筒量程选择的依据有两点:一是保证测量一次,二是量程要与液体的取用量最接近,故做某实验量取47mL的水,应选用的量筒是50mL,当加入的液体量接近刻度线时,要改用滴管滴加液体.
故选:C.
点评 量筒的使用是中考热点之一,掌握量筒的使用方法、量程的选择方法等是正确解答本题的关键.

练习册系列答案
相关题目
8.通过观察实验现象获得证据,从而归纳出相关结论是科学上常用的研究方法,下列实验现象和对应的结论正确的是( )
| A. | 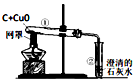 试管①红色粉末变成黑色,试管②的澄清石灰水变浑浊,说明碳具有还原性 | |
| B. |  铁丝表面覆盖红色物质,溶液由蓝色逐渐变成无色,说明铁的金属活动性强于铜 | |
| C. |  烧杯中的红色溶液逐渐变浅最后变成无色,说明盐酸与氢氧化钠能发生反应 | |
| D. | 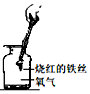 铁丝在氧气中剧烈燃烧、火星四射,生成的黑色物质是氧化铁 |
13.由A、B两种元素组成的物质中,A、B元素的相对原子质量比7:2,A、B元素的质量比7:3,则该物质是( )
| A. | A2B | B. | A2B3 | C. | AB2 | D. | A3B2 |
7.为了除去粗盐中的Ca2+、Mg2+、SO42-及泥砂,可将粗盐溶于水,然后进行下列五项操作①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液.下列操作顺序中最合适的是( )
| A. | ①④②⑤③ | B. | ④①②⑤③ | C. | ②⑤④①③ | D. | ⑤②④③① |
8.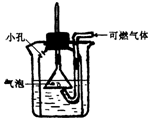 如图是某同学设计的一个可燃气体安全点燃装置,对此装置的评价和使用错误的是( )
如图是某同学设计的一个可燃气体安全点燃装置,对此装置的评价和使用错误的是( )
 如图是某同学设计的一个可燃气体安全点燃装置,对此装置的评价和使用错误的是( )
如图是某同学设计的一个可燃气体安全点燃装置,对此装置的评价和使用错误的是( )| A. | 未经检验纯度的气体通过此装置后可安全点燃,不会发生爆炸 | |
| B. | 此装置防止点燃不纯气体爆炸的原理是使不纯的气体不与燃着气体直接接触 | |
| C. | 要达到安全点燃效果,烧杯内的水可不没过倒置漏斗的边缘 | |
| D. | 此装置适用于难溶于水的可燃性气体 |

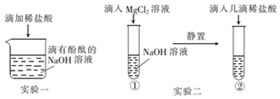 实验小组在探究“酸与碱能否发生反应”时,进行了如图所示实验.请根据实验回答:
实验小组在探究“酸与碱能否发生反应”时,进行了如图所示实验.请根据实验回答: