题目内容
3.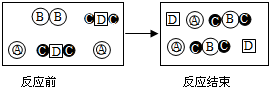 如图为一组物质发生化学反应的示意图,A、B、C、D分别表示不同原子.在下列从图中获得的信息中,一定错误的是( )
如图为一组物质发生化学反应的示意图,A、B、C、D分别表示不同原子.在下列从图中获得的信息中,一定错误的是( )| A. | 反应前物质的组成是混合物 | B. | 反应过程中D元素的化合价不变 | ||
| C. | A原子构成的单质可能是催化剂 | D. | 反应前后原子总数不变 |
分析 根据图示的含义写出反应的方程式为B2+2C2D=2D+2C2B,结合反应的特点分析反应类型,催化剂的定义、物质的分类等进行分析.
解答 解:根据微观示意图分析分子的结构,可知反应的方程式为:B2+2C2D=2D+2C2B,因此:
A、由图示可知,反应前是由三种物质组成的混合物,故说法正确;
B、反应过程中D元素由化合物的形式变为了单质的形式,化合价一定改变变,故说法错误;
C、A原子构成的单质在反应前后不变,故可能是该反应的催化剂也可能与反应无关,故说法正确;
D、由图示可知,反应前后原子总数不变,故说法正确;
故选项为:B.
点评 该题不仅考查了学生对化学知识的掌握情况,还考查了学生观察理解微观模型示意图的能力,从多方面考查了学生的综合能力.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
11.联合国环境规划署宣布,今年6月5日世界环境日主题是“绿色经济:你参与了吗?”旨在推动人们思考如何让绿色经济深入到日常生活的方方面面,并以此带来社会、经济和环境方面的良性转变,从而满足世界人口不断增长的需要.下列做法中正确的是( )
| A. | 尽可能用太阳能热水器代替燃气热水器 | |
| B. | 将废电池和生活垃圾一起丢进垃圾箱 | |
| C. | 在旱地上进行大规模的农牧业生产活动 | |
| D. | 将工业的废水和生活的污水大量排入江河湖泊 |
18. CaCO3广泛存在于自然界,是一种重要的化工原料.某种大理石除主要成分为CaCO3外,还有少量的硫化物.某同学用这种大理石和稀盐酸反应,开展以下探究:
CaCO3广泛存在于自然界,是一种重要的化工原料.某种大理石除主要成分为CaCO3外,还有少量的硫化物.某同学用这种大理石和稀盐酸反应,开展以下探究:
【查阅资料】
资料一:已知碳酸钙与盐酸的复分解反应可自发进行.在常温下,测得浓度均为a%的下列五种溶液的pH大小情况:
表中pH大小情况揭示出复分解反应的一条规律:较强酸发生类似反应可以生成较弱酸.下列反应中不符合该规律的是D(填字母)
A、H2SO4+Na2CO3=2NaCl+2H2O+2CO2↑ B、2HCl+CaS=CaCl2+H2S↑
C、CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO D、H2S+CuSO4=H2SO4+CuS↓
资料二:常见干燥剂有①五氧化二磷②无水氯化钙③碱石灰④生石灰⑤浓硫酸
【实验探究】
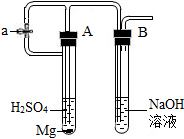
为了得到纯净的二氧化碳,设计了如图装置,请你分析:
a.制备的CO2气体中,可能含有的杂质是HCl、H2S、和水蒸气;
b.上述装置中,A是CuSO4溶液,B物质的名称可能是无水氯化钙(或五氧化二磷);
c.用这个实验得到的气体测定CO2的相对分子质量,如果B物质失效,测定结果偏高(填“偏高”、“偏低”或“不受影响”).
 CaCO3广泛存在于自然界,是一种重要的化工原料.某种大理石除主要成分为CaCO3外,还有少量的硫化物.某同学用这种大理石和稀盐酸反应,开展以下探究:
CaCO3广泛存在于自然界,是一种重要的化工原料.某种大理石除主要成分为CaCO3外,还有少量的硫化物.某同学用这种大理石和稀盐酸反应,开展以下探究:【查阅资料】
资料一:已知碳酸钙与盐酸的复分解反应可自发进行.在常温下,测得浓度均为a%的下列五种溶液的pH大小情况:
| 溶质 | H2SO4 | HCl | H2S | H2CO3 | HClO |
| pH | 小→大 | ||||
A、H2SO4+Na2CO3=2NaCl+2H2O+2CO2↑ B、2HCl+CaS=CaCl2+H2S↑
C、CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO D、H2S+CuSO4=H2SO4+CuS↓
资料二:常见干燥剂有①五氧化二磷②无水氯化钙③碱石灰④生石灰⑤浓硫酸
【实验探究】
为了得到纯净的二氧化碳,设计了如图装置,请你分析:
a.制备的CO2气体中,可能含有的杂质是HCl、H2S、和水蒸气;
b.上述装置中,A是CuSO4溶液,B物质的名称可能是无水氯化钙(或五氧化二磷);
c.用这个实验得到的气体测定CO2的相对分子质量,如果B物质失效,测定结果偏高(填“偏高”、“偏低”或“不受影响”).
15.某同学用氯化钠固体和蒸馏水配制氯化钠溶液.他往95毫升水(密度为1g/cm3)中加入5克氯化钠固体,配制成了实验需要的溶液,把溶液全部装入试剂瓶后,贴上标签.该标签的书写正确的是( )
| A. |  | B. |  | C. |  | D. |  |
4.最近,科学家制造出了含4个氧原子的新型“氧分子”,而氧分子是由2个氧原子构成的,针对以上事实,下列有关说法错误的是( )
| A. | 氧气的分子结构与新型“氧分子”的结构应该相同 | |
| B. | 氧气的分子结构与新型“氧分子”的物理性质应该不同 | |
| C. | 新型“氧分子”与氧分子都是由氧原子构成的 | |
| D. | 每个新型氧分子与每个氧气分子含有的氧原子数不同 |
 2014年,黑龙江省的粮食产量又跃居全国第一,如图是某农场的一块麦田,请回答有关问题:
2014年,黑龙江省的粮食产量又跃居全国第一,如图是某农场的一块麦田,请回答有关问题: