题目内容
1.将足量的稀盐酸加入一定量的铁、铜混合物中,写出其中反应的化学方程式Fe+2HCl=FeCl2+H2↑.图7是实验过程生成气体或剩余固体的质量随反应时间的变化关系,其中表示正确的是A、C(填标号).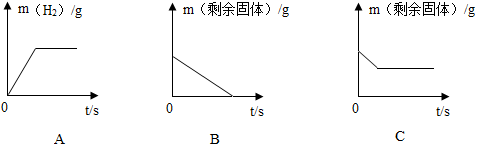
分析 根据金属的活动性顺序以及反应过程来分析,氢前面的金属能置换出盐酸、硫酸中的氢.
解答 解:根据金属的活动性顺序可知,铁与稀盐酸反应生成氯化亚铁和氢气,而铜与稀盐酸不反应;反应的方程式是:Fe+2HCl=FeCl2+H2↑;随着反应的进行,氢气的质量增加,当铁完全反应后,氢气的质量不再改变;随着铁的反应,金属混合物的质量不断减小,当铁完全反应后,剩余固体是铜,质量不再减小.所以AC正确.
故答为:Fe+2HCl=FeCl2+H2↑; A、C.
点评 本题考查学生对金属的性质及金属锈蚀的条件及其防护措施的理解与在解题、生活中应用的能力.

练习册系列答案
相关题目
11.下列是2016年我省新增的国家地理标志保护产品中的4个,其中富含蛋白质的是( )
| A. |  来安花红(沙果) | B. |  明光绿豆 | C. |  运漕酒 | D. |  龙池尖茶 |
12.下列实验操作、现象与结论对应关系正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用黄铜片在铜片上刻画 | 铜片上有划痕 | 黄铜的硬度比铜大 |
| B | 将燃烧着的木条伸入到盛气体的集气瓶中 | 燃烧着的木条熄灭 | 瓶中一定是二氧化碳气体 |
| C | 向某水样加入少量肥皂水 | 有大量泡沫产生 | 该水样一定是纯净水 |
| D | 锌粉和铝片中分别滴入同种稀硫酸 | 锌粉放出气体的速度更快 | 锌金属活动性比铝强 |
| A. | A | B. | B | C. | C | D. | D |
7.3月29日是本年度的“地球一小时”(Earth Hour)活动日,主题为“蓝天自造”,旨在呼吁每一位公民从自身开始,采取实际行动,应对当前中国最紧迫、最受关注的环境议题--雾霾.作为一名中学生,下列做法不符合这一主题的是( )
| A. | 选择自行车和公交车作为出行工具 | |
| B. | 将废纸、汽水瓶等收集起来,一次性焚烧 | |
| C. | 让衣服自然晾干,节约用纸,不使用一次性塑料袋 | |
| D. | 拒绝使用一次性木筷,用电子贺卡代替纸制贺卡 |
4.关于水的蒸发过程,下列说法正确的是( )
| A. | 水分子之间间隔增大 | B. | 水分子体积增大 | ||
| C. | 水分子质量增加 | D. | 水分子个数增多 |
5.有关金属资源的叙述正确的是( )
| A. | 地球上金属资源是有限的,而且不能再生 | |
| B. | 目前世界产量最高的金属是铝 | |
| C. | 保护金属资源的唯一途径是防止金属腐蚀 | |
| D. | 地球上金属资源大多数以单质形式存在,如金、银、铜 |