题目内容
15.高铁酸钠(Na2FeO4)是一种新型高效的水处理剂,下列有关高铁酸钠的说法正确的是( )| A. | 属于氧化物 | |
| B. | 钠、铁、氧三种元素的质量比为2:1:4 | |
| C. | 钠元素的质量分数最高 | |
| D. | 铁元素的化合价为+6价 |
分析 A.根据氧化物的概念来分析;
B.根据化合物中元素质量比的计算方法来分析;
C.根据化合物中元素质量分数大小比较方法来分析;
D.根据化合物中元素化合价的计算方法来分析.
解答 解:A.高铁酸钠是由钠、铁、氧三种元素组成的化合物,而氧化物中只含两种元素,故不属于氧化物,故错误;
B.高铁酸钠中钠、铁、氧三种元素质量比是(23×2):56:(16×4)≠2:1:4,故错误;
C.高铁酸钠中钠、铁、氧三种元素质量比是(23×2):56:(16×4)=46:56:64,由此可见其中氧元素的质量分数最大,故错误;
D.化合物中各元素化合价代数和为零,钠显+1价,氧显-2价,因此高铁酸钠中铁元素的化合价为+6价,故正确.
故选D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
20.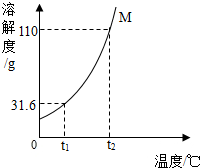 如图是M物质的溶解度曲线.在t2℃时,将110克M物质配制成饱和溶液,将其降温至t1℃时,理论上所得溶液的质量为( )
如图是M物质的溶解度曲线.在t2℃时,将110克M物质配制成饱和溶液,将其降温至t1℃时,理论上所得溶液的质量为( )
 如图是M物质的溶解度曲线.在t2℃时,将110克M物质配制成饱和溶液,将其降温至t1℃时,理论上所得溶液的质量为( )
如图是M物质的溶解度曲线.在t2℃时,将110克M物质配制成饱和溶液,将其降温至t1℃时,理论上所得溶液的质量为( )| A. | 210克 | B. | 110克 | C. | 31.6克 | D. | 131.6克 |
5.某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验,向烧杯中的氢氧化钙溶液中滴加一定量的稀盐酸后,发现忘记滴加指示剂,此时,他们停止滴加稀盐酸,并对烧杯内溶液中溶质的成分进行研究.
(1)写出该中和反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
(2)探究烧杯内溶液中溶质的成分:
【作出猜想】(A)溶质可能是CaCl2与Ca(OH)2 (B)溶质可能是CaCl2 (C)溶质可能是CaCl2与HCl
【查阅资料】CaCl2溶液呈中性
【实验设计】
①取少量烧杯中的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是排除了猜想(A),你认为排除猜想(A)的理由是氢氧化钙溶液呈碱性,使酚酞试液变红,现不变红,故溶质不可能含氢氧化钙.
②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写表格:
通过以上探究,最后确定猜想(C)正确.
【反思与拓展】你认为上述烧杯内溶液如果未经处理直接倒入铁质下水管道,可能造成的危害是腐蚀铁质下水道
水污染,要想处理烧杯内溶液使其只得到CaCl2溶液,应向溶液中加入过量的石灰石,充分反应后过滤,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(1)写出该中和反应的化学方程式Ca(OH)2+2HCl═CaCl2+2H2O.
(2)探究烧杯内溶液中溶质的成分:
【作出猜想】(A)溶质可能是CaCl2与Ca(OH)2 (B)溶质可能是CaCl2 (C)溶质可能是CaCl2与HCl
【查阅资料】CaCl2溶液呈中性
【实验设计】
①取少量烧杯中的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.于是排除了猜想(A),你认为排除猜想(A)的理由是氢氧化钙溶液呈碱性,使酚酞试液变红,现不变红,故溶质不可能含氢氧化钙.
②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写表格:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量反应后的溶液与试管中,逐滴加入碳酸钠溶液 | 产生沉淀 | 猜想(B)正确 |
| 先产生气泡,后产生沉淀 | 猜想(C)正确 |
【反思与拓展】你认为上述烧杯内溶液如果未经处理直接倒入铁质下水管道,可能造成的危害是腐蚀铁质下水道
水污染,要想处理烧杯内溶液使其只得到CaCl2溶液,应向溶液中加入过量的石灰石,充分反应后过滤,反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.