题目内容
14.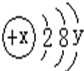 某粒子的结构示意图如图
某粒子的结构示意图如图(1)若该粒子为一稀有气体元素的原子,则x=18,y=8.
(2)若该粒子为R2+,则x=20,y=8.
(3)若该粒子为Mn-,则x=18-n,y=8.
分析 根据已有的粒子的结构示意图结合原子得失电子形成阴阳离子的知识进行分析解答即可.
解答 解:(1)该粒子为一稀有气体元素的原子,则最外层电子数为8,故x=2+8+8=18,故填:18,8;
(2)该粒子为R2+,则是失去两个电子形成的,y是8,故x=2+8+8+2=20,故填:20,8;
(3)该粒子为Mn-,则是得到n个电子形成的,y是8,故x=2+8+8-n=18-n,故填:18-n,8.
点评 解答本题的关键是知道原子和离子中质子数与核外电子数的关系.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目
2.安徽物产丰富.以下安徽名产中不含有机物的是( )
| A. |  名茶-黄山银勾 | B. |  名食-涂山农家圆子 | ||
| C. |  名酒-淮北口子窖 | D. |  名砚-歙县龙尾砚 |
3.稀盐酸中混有少量硫酸,为了除去硫酸,可加入适量( )
| A. | 铁屑 | B. | 氯化钡溶液 | C. | 硝酸银溶液 | D. | 氢氧化钠溶液 |
2.下列化学方程式中正确的是( )
| A. | Fe2O3+4HCl═2FeCl2+2H2O | B. | CO+CuO═Cu+CO2 | ||
| C. | 2KOH+SO2═K2SO4+H2O | D. | 4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 |
4.推理是化学学习中常用的思维方法.下列推理正确的是( )
| A. | 酸能使紫色石蕊溶液变红.通入CO2后的紫色石蕊溶液变红,所以CO2是酸 | |
| B. | 酸性溶液的pH小于7.食醋是酸性溶液,所以食醋的pH小于7 | |
| C. | 在同一化合物中,金属元素显正价,所以非金属元素一定显负价 | |
| D. | 可用灼热的碳除去二氧化碳中的氧气 |