题目内容
为了除去氯化钠样品中的碳酸钠杂质,兴趣小组最初设计了如图的方案并进行实验.
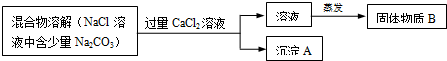
(1)写出沉淀A的化学式 .
(2)加入CaCl2溶液后,分离得到沉淀A的实验操作方法是 .
(3)同学在实验过程中,又发现了新的问题:此方案很容易引入新的杂质,请写出固体物质B的成分 (用化学式表示).

(1)写出沉淀A的化学式
(2)加入CaCl2溶液后,分离得到沉淀A的实验操作方法是
(3)同学在实验过程中,又发现了新的问题:此方案很容易引入新的杂质,请写出固体物质B的成分
考点:物质除杂或净化的探究,盐的化学性质
专题:物质的分离、除杂、提纯与共存问题
分析:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答:解:(1)碳酸钠溶液能与过量氯化钙溶液反应生成碳酸钙沉淀和氯化钠,故沉淀A为碳酸钙,其化学式为:CaCO3.
(2)加入CaCl2溶液后,分离得到沉淀A(碳酸钙),可采用过滤的方法.
(3)过滤后,所得滤液中含有氯化钠、氯化钙(过量的),故溶液蒸发后固体物质B的成分是氯化钠、氯化钙,其化学式分别是NaCl、CaCl2.
故答案为:(1)CaCO3;(2)过滤;(3)NaCl、CaCl2.
(2)加入CaCl2溶液后,分离得到沉淀A(碳酸钙),可采用过滤的方法.
(3)过滤后,所得滤液中含有氯化钠、氯化钙(过量的),故溶液蒸发后固体物质B的成分是氯化钠、氯化钙,其化学式分别是NaCl、CaCl2.
故答案为:(1)CaCO3;(2)过滤;(3)NaCl、CaCl2.
点评:物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目

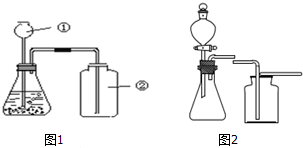
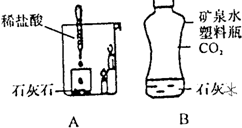 如图是验证二氧化碳性质的实验:
如图是验证二氧化碳性质的实验: