题目内容
12. 如图是初中化学所学的常见化合物之间的相互转化关系(反应条件和生成产物中的水已略去),其中A是一种常见的建筑材料,B是一种常见的气体,H是一种含钠的化合物.
如图是初中化学所学的常见化合物之间的相互转化关系(反应条件和生成产物中的水已略去),其中A是一种常见的建筑材料,B是一种常见的气体,H是一种含钠的化合物.请回下列问题:
(1)写出A、D、H的化学式:ACaCO3;DNaOH;HNaCl.
(2)E物质属于盐(填“酸”、“碱”、“盐”或“”氧化物).
(3)B物质和G物质发生化学反应的现象是有白色沉淀生成.
(4)写出下列反应的化学方程式:
①A发生化学反应生成B和CCaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
②C和F反应CaO+H2O=Ca(OH)2.
分析 根据A是一种常见建筑材料的主要成分,A又会分解成B和C,所以A就是碳酸钙,B是一种常见的气体,B就是二氧化碳,所以C就是氧化钙,H是一种含钠的化合物,E和盐酸会生成H和二氧化碳,所以E就是碳酸钠,D就是氢氧化钠,H就是氯化钠,碳酸钠和G会生成A碳酸钙和D氢氧化钠,所以G就是氢氧化钙,F就是水,将推出的各物质代入转换关系中进行验证即可.
解答 解:(1)A是一种常见建筑材料的主要成分,A又会分解成B和C,所以A就是碳酸钙,B是一种常见的气体,B就是二氧化碳,所以C就是氧化钙,H是一种含钠的化合物,E和盐酸会生成H和二氧化碳,所以E就是碳酸钠,D就是氢氧化钠,H就是氯化钠,碳酸钠和G会生成A碳酸钙和D氢氧化钠,所以G就是氢氧化钙,F就是水,经过验证,推导正确,所以A是CaCO3,D是NaOH,H是NaCl;
(2)通过推导可知,E是碳酸钠,属于盐;
(3)B物质和G物质发生的反应是氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,实验现象是:有白色沉淀生成;
(4)①A发生化学反应生成B和C的反应是碳酸钙在高温的条件下生成氧化钙和二氧化碳,化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
②C和F反应的反应是氧化钙和水反应生成氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2.
故答案为:(1)CaCO3,NaOH,NaCl;
(2)盐;
(3)有白色沉淀生成;
(4)①CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
②CaO+H2O=Ca(OH)2.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案| A. | 静置 | B. | 过滤 | C. | 吸附 | D. | 蒸馏 |
| A. | 镁离子Mg-2 | B. | 5个水分子5H2O | ||
| C. | 天然气的主要成分是CO | D. | 地壳中含量最多的金属元素Fe |
| A. | 用肥皂水检验软水和硬水 | |
| B. | 用火柴检查天然气管道有无泄漏 | |
| C. | 冷碟子放在蜡烛火焰上方,得到炭黑 | |
| D. | 用灼烧的方法区别棉花和羊毛 |
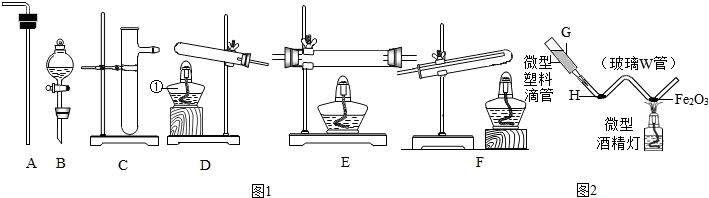
| A. | 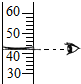 量取液体 | B. | 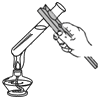 加热液体 | C. | 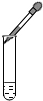 滴加液体 | D. | 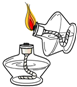 点酒精灯 |
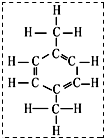 对二甲苯(简称PX):无色透明液体,具有芳香气味,能与乙醇等有机溶剂混溶,可燃,低毒,毒性略高于乙醇,其蒸气与空气可形成爆炸性混合物.如图是“PX”的结构式,下列有关“PX”的说法不正确的是( )
对二甲苯(简称PX):无色透明液体,具有芳香气味,能与乙醇等有机溶剂混溶,可燃,低毒,毒性略高于乙醇,其蒸气与空气可形成爆炸性混合物.如图是“PX”的结构式,下列有关“PX”的说法不正确的是( )| A. | “PX”属于有机化合物 | B. | “PX”的化学式为C8H10 | ||
| C. | “PX”中C、H两种元素的质量比为4:5 | D. | “PX”完全燃烧后产生二氧化碳和水 |
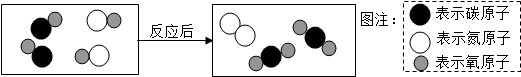
| A. | 图中所示反应基本类型为置换反应 | B. | 反应前后有的元素化合价发生改变 | ||
| C. | 图中所示有三种氧化物 | D. | 反应前后原子种类、个数均不改变 |
 2015年5月31日凌晨,在国际田联钻石联赛尤金站比赛中,中国飞人苏炳添在男子100米比赛中,以9秒99的成绩并列获得季军,苏炳添就此成为历史上首位突破10秒大关的黄种人,他也创造了新的全国纪录,他是黄种人的骄傲.
2015年5月31日凌晨,在国际田联钻石联赛尤金站比赛中,中国飞人苏炳添在男子100米比赛中,以9秒99的成绩并列获得季军,苏炳添就此成为历史上首位突破10秒大关的黄种人,他也创造了新的全国纪录,他是黄种人的骄傲.