题目内容
13.下列不包含化学变化的是( )| A. |  铁生锈 | B. |  二氧化碳性质探究 | ||
| C. |  洗涤剂洗碗 | D. |  分子性质探究 |
分析 化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.
解答 解:A、铁生锈过程中有新物质铁锈生成,属于化学变化.
B、二氧化碳性质探究过程中,二氧化碳溶于水生成碳酸,有新物质生成,属于化学变化.
C、洗涤剂洗碗是利用了洗涤剂的乳化作用,没有新物质生成,属于物理变化.
D、分子性质探究过程中酚酞溶液遇浓氨水变色,有新物质生成,属于化学变化.
故选C.
点评 本题难度不大,解答时要分析变化过程中是否有新物质生成,若没有新物质生成属于物理变化,若有新物质生成属于化学变化.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.如图所示,氢原子结构的各种模型图,其中正确的是( )
| A. |  | B. | 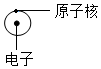 | C. | 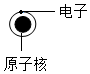 | D. |  |
8.软锰矿的主要成分是MnO2,还含有少量重金属化合物等杂质.黄铁矿的 主要成分是FeS2,还含有硅、铝的氧化物等杂质.工业上采用同槽酸浸工艺制备碳酸锰并回收硫酸铵,其主要流程如下:
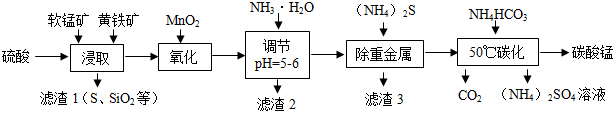
资料:Ⅰ.“氧化”时发生反应:MnO2+2FeSO4+2H2SO4=Fe2(SO4)3+MnSO4+2H2O
Ⅱ.部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH见表:
请回答:
(1)为了提高锰元素的浸出率,在“浸取”时可采取的措施有:①适当升高温度;②搅拌;③加入足量硫酸;
(2)“滤渣2”中主要成分的化学式为Al(OH)3、Fe(OH)3;
(3)“除重金属”时使用(NH4)2S而不使用Na2S的原因是能够防止带入钠离子;
(4)“50℃碳化”得到碳酸锰,反应的化学方程式为MnSO4+2NH4HCO3=MnCO3+(NH4)2SO4+H2O+CO2↑;
(5 )生成的碳酸锰产品需经充分洗涤,检验产品完全洗净的方法是取最后一次洗涤液,加入氯化钡溶液,不产生沉淀.

资料:Ⅰ.“氧化”时发生反应:MnO2+2FeSO4+2H2SO4=Fe2(SO4)3+MnSO4+2H2O
Ⅱ.部分金属阳离子以氢氧化物形式完全沉淀时溶液的pH见表:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 10.4 |
(1)为了提高锰元素的浸出率,在“浸取”时可采取的措施有:①适当升高温度;②搅拌;③加入足量硫酸;
(2)“滤渣2”中主要成分的化学式为Al(OH)3、Fe(OH)3;
(3)“除重金属”时使用(NH4)2S而不使用Na2S的原因是能够防止带入钠离子;
(4)“50℃碳化”得到碳酸锰,反应的化学方程式为MnSO4+2NH4HCO3=MnCO3+(NH4)2SO4+H2O+CO2↑;
(5 )生成的碳酸锰产品需经充分洗涤,检验产品完全洗净的方法是取最后一次洗涤液,加入氯化钡溶液,不产生沉淀.
18.下列事实的微观解释不正确的是( )
| 选项 | 事实 | 解释 |
| A | 硫化氢是有毒气体 | 硫化氢分子是有毒的 |
| B | 架在高处的电线夏季变得比冬季长 | 夏季温度高原子间间隔变大 |
| C | 氯化铜与氢氧化钙两溶液间的反应速率比两固体间的反应快 | 参加反应的粒子在溶液中接触机会比在固体中接触机会多 |
| D | 酒精溶液不导电 | 酒精溶液中没有自由移动的粒子 |
| A. | A | B. | B | C. | C | D. | D |
2.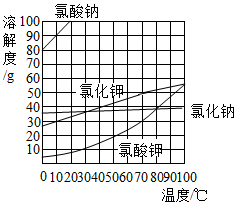 根据如图提供的几种物质的溶解度曲线,判断下列说法正确的是( )
根据如图提供的几种物质的溶解度曲线,判断下列说法正确的是( )
 根据如图提供的几种物质的溶解度曲线,判断下列说法正确的是( )
根据如图提供的几种物质的溶解度曲线,判断下列说法正确的是( )| A. | 氯酸钾中混有少量氯化钠,提纯氯酸钾最好用蒸发结晶的方法 | |
| B. | 30℃氯酸钾饱和溶液的溶质质量分数为10% | |
| C. | 80℃时7gNaCl和20g水能形成饱和溶液 | |
| D. | 控制温度,图中氯酸钠和氯化钾能发生化学反应 |
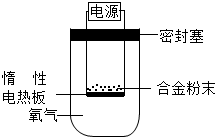 镁是一种活泼金属,除了能与氧气反应,还可以与氮气、二氧化碳等反应.为测定镁铝合金(不含其他元素)中镁的质量分数,称量ag镁铝合金粉末,放在如图所示装置的惰性电热板上,通电使其充分灼烧.下列关于该实验的说法正确的是( )
镁是一种活泼金属,除了能与氧气反应,还可以与氮气、二氧化碳等反应.为测定镁铝合金(不含其他元素)中镁的质量分数,称量ag镁铝合金粉末,放在如图所示装置的惰性电热板上,通电使其充分灼烧.下列关于该实验的说法正确的是( )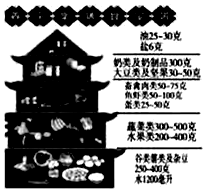 我们每天摄入的食物不仅要保证一定的数量,还要注意合理搭配,以保证各种营养素的均衡摄入.“营养平衡膳食宝塔”为我们提供了合理选择食物的指南.请回答问题:
我们每天摄入的食物不仅要保证一定的数量,还要注意合理搭配,以保证各种营养素的均衡摄入.“营养平衡膳食宝塔”为我们提供了合理选择食物的指南.请回答问题:
