题目内容
14.有一白色固体X,其主要成分是氯化钠,可能含有碳酸钙、氯化钙、硫酸铜和氢氧化钙中的一种或几种,为探究其组成进行如图实验,主要流程及现象记录如图(提示:氢化钙溶液呈中性)
根据流程图回答下列问题
(1)根据步骤①的实验现象,确定白色固体X中一定没有的物质是硫酸铜.
(2)步骤②中发生反应的化学方程式是CaCO3+2HCl=CaCl2+CO2↑+H2O.
(3)步骤③中产生白色沉淀A的化学方程式是CaCl2+Na2CO3═CaCO3↓+2NaCl.
(4)白色固体X中含有的物质是氯化钠、碳酸钙和氯化钙.
分析 根据碳酸钙难溶于水,硫酸铜溶液为蓝色,再根据图框可知:得无色溶液,推测白色固体X中一定没有的物质是硫酸铜,而白色沉淀与稀盐酸反应生成无色气体,推测含有碳酸根;而步骤③中产生白色沉淀A的反应为氯化钙与碳酸钠溶液的反应进行分析.
解答 解:因为碳酸钙难溶于水,硫酸铜溶液为蓝色,再根据图框可知:得无色溶液,推测白色固体X中一定没有的物质是硫酸铜,而白色沉淀与稀盐酸反应生成无色气体,推测含有碳酸根;而步骤③中产生白色沉淀A的反应为氯化钙与碳酸钠溶液的反应,所以:
(1)根据步骤①实验现象确定白色固体X中一定没有的物质是硫酸铜;
(2)步骤②中发生的反应是碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式是:CaCO3+2HCl=CaCl2+CO2↑+H2O;
(3)步骤③中产生白色沉淀是氯化钙和碳酸钠反应产生碳酸钙沉淀和氯化钠,化学方程式为:CaCl2+Na2CO3═CaCO3↓+2NaCl;
(4)通过推导可知,白色固体X中的物质有:氯化钠、碳酸钙和氯化钙.
故答案为:(1)硫酸铜;
(2)CaCO3+2HCl=CaCl2+CO2↑+H2O;
(3)CaCl2+Na2CO3═CaCO3↓+2NaCl;
(4)氯化钠、碳酸钙和氯化钙.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
7.小明的邻居张大爷种植蔬菜,现在他有点苦恼,去年购买的化肥,由于外包装上的字迹看不清,只记得该化肥是硫酸钾、碳酸氢铵、氯化铵中的一种.小明利用学过的化学知识,设计如下实验方案帮张大爷鉴别化肥:
【实验步骤】取上述化肥少量于一容器中,加入少量熟石灰粉末,混合研磨.
【实验现象】嗅到氨气的刺激性气味.
【实验结论】小明由上述实验推断该化肥不是硫酸钾.
(1)请根据上述实验结论,设计一个简单的实验方案来进一步证明该化肥可能是什么.
(2)实验室检验氨气的方法是用湿润的红色石蕊试纸检验,试纸变蓝证明有氨气.
(3)通过小明的实验,请你写出使用铵态氮肥的一点注意事项:严禁与碱性肥料混合使用.
【实验步骤】取上述化肥少量于一容器中,加入少量熟石灰粉末,混合研磨.
【实验现象】嗅到氨气的刺激性气味.
【实验结论】小明由上述实验推断该化肥不是硫酸钾.
(1)请根据上述实验结论,设计一个简单的实验方案来进一步证明该化肥可能是什么.
| 实验步骤 | 实验现象 | 结论或有关化学反应方程式 |
| 取少量样品放于试管中,加入少量稀盐酸 | 产生气泡,该气体能使澄清石灰水变浑浊 | 该化肥是碳酸氢铵 (或HCl+NH4HCO3═NH4Cl+H2O+CO2↑ CO2+Ca(OH)2═CaCO3↓+H2O) |
(3)通过小明的实验,请你写出使用铵态氮肥的一点注意事项:严禁与碱性肥料混合使用.
2.下列变化属于化学变化的是( )
| A. | 冰雪融化 | B. | 葡萄酿酒 | C. | 酒精挥发 | D. | 铁水铸锅 |
9.下列叙述不符合实验事实的是( )
| A. | 向CaCl2溶液中溶入CO2气体,会产生白色沉淀 | |
| B. | 久置于空气中的熟石灰,加入足量稀盐酸会有气泡产生 | |
| C. | 向滴有石蕊试液的蒸馏水中加入Fe(OH)3,溶液显蓝色 | |
| D. | 向Na2CO3、K2SO4溶液中分别滴加BaCl2溶液,都会产生白色沉淀 |
19. 随着经济的发展,能源与环境成为人们日益关注的问题.
随着经济的发展,能源与环境成为人们日益关注的问题.
(1)6月5日是世界环境日,下列有关环境的说法错误的是AD.
A.焚烧塑料是减少白色污染的有效方法
B.废旧电池随手丢弃会造成地下水及土壤污染
C.空气中O3含量超标会引起温室效应
D.化工厂可通过加高烟囱排放废气,防止空气污染
(2)酸雨是由SO2、NO2(或硫和氮的氧化物)气体或这些气体在空气中反应后的生成物溶于雨水所形成.A、B、C三个地区雨水的pH如图所示,其中BC地区的雨水是酸雨.
(3)如表是煤的一种综合利用方式.甲、乙、丙、丁分别表示四种物质,在一定条件下,甲+乙→丙+丁.它们的部分化学式和微观示意图分别列于表:
①写出甲物质的化学式H2O,画出丁物质的微观示意图 .
.
②在上述反应中提供氧,具有氧化性的物质为甲.
 随着经济的发展,能源与环境成为人们日益关注的问题.
随着经济的发展,能源与环境成为人们日益关注的问题.(1)6月5日是世界环境日,下列有关环境的说法错误的是AD.
A.焚烧塑料是减少白色污染的有效方法
B.废旧电池随手丢弃会造成地下水及土壤污染
C.空气中O3含量超标会引起温室效应
D.化工厂可通过加高烟囱排放废气,防止空气污染
(2)酸雨是由SO2、NO2(或硫和氮的氧化物)气体或这些气体在空气中反应后的生成物溶于雨水所形成.A、B、C三个地区雨水的pH如图所示,其中BC地区的雨水是酸雨.
(3)如表是煤的一种综合利用方式.甲、乙、丙、丁分别表示四种物质,在一定条件下,甲+乙→丙+丁.它们的部分化学式和微观示意图分别列于表:
| 物质 | 甲 | 乙 | 丙 | 丁 | 图例: |
| 化学式 | ? | C | ? | H2 | |
| 微观示意图 |  |  |  | ? |
 .
.②在上述反应中提供氧,具有氧化性的物质为甲.
6.下列实验操作不能达到实验目的是
( )
| 物质 | 实验目的 | 实验操作 | |
| A | MnO2和C粉末 | 检验MnO2 | 分别滴加双氧水 |
| B | 硬水和软水 | 鉴别 | 加肥皂水,搅拌,观察产生泡沫的多少 |
| C | Cu粉中含有少量Fe粉 | 除去Fe粉 | 加入足量稀硫酸、过滤 |
| D | 固体KNO3中含少量NaCl | 除去NaCl | 溶解、过滤、蒸发 |
| A. | A | B. | B | C. | C | D. | D |
3.下列实验方法中,一定能达到实验目的是( )
| 选项 | 实验目的 | 实验方法 |
| A | 检验一瓶气体是否为CO2 | 将带火星的木条伸入瓶中 |
| B | 鉴别NaCl溶液和稀盐酸 | 滴加无色酚酞溶液 |
| C | 分离碳酸钠和氢氧化钠的混合物 | 加入过量氢氧化钙溶液,过滤 |
| D | 验证物质燃烧条件之一是温度达到着火点 | 用导管分别对准浸没在热水和冷水中的白磷通氧气 |
| A. | A | B. | B | C. | C | D. | D |
3.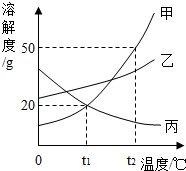 如图是甲、乙、丙三种固体物质的溶解度曲线.下列说法错误是( )
如图是甲、乙、丙三种固体物质的溶解度曲线.下列说法错误是( )
 如图是甲、乙、丙三种固体物质的溶解度曲线.下列说法错误是( )
如图是甲、乙、丙三种固体物质的溶解度曲线.下列说法错误是( )| A. | t1℃时,甲、丙两种物质的饱和溶液溶质质量分数相同 | |
| B. | t2℃时,30g甲加入到50g水中充分溶解,所得溶液中溶质质量分数为37.5% | |
| C. | 要从甲物质的饱和溶液中获得晶体甲,可以采用降温的方法 | |
| D. | 将三种物质的饱和溶液从t2℃降温至t1℃,所得溶液中溶质质量分数乙>甲>丙 |