题目内容
3.如图是小华同学用氢氧化钠固体和水配制500g溶质质量分数2.5%的NaOH溶液的操作过程,该同学在称量氢氧化钠时,先将天平调节平衡,然后在两个托盘上各放一张质量相同的纸,把药品直接放在纸上称量.
(1)根据上述实验,请回答:
①a操作的错误是氢氧化钠直接放在纸上称量.
②下列操作中导致溶质质量分数偏低的是AB(填字母).
A.a操作中砝码和氢氧化钠放错盘 B.b中烧杯用水洗涤后未干燥就使用
C.c操作中视线与量筒凹液面最低处保持水平 D.d操作中有少量水溅出
(2)小华在测定所配制溶液的酸碱度时,先将pH试纸用蒸馏水湿润,再进行测定,则测的溶液的pH值偏小(选填“偏大”、“偏小”或“不受影响”).
(3)小华将上述溶液稀释成0.2%做电解水实验,用带火星的木条检验正极产生的气体.若将100g稀释后的氢氧化钠溶液电解,实验后溶液中氢氧化钠的质量分数变为0.25%,有20g水被电解.(已知氢氧化钠可增强水的导电性,在通电前后质量不变)
分析 (1)①根据氢氧化钠具有腐蚀性不能放在纸上称量考虑;②根据导致溶质质量分数偏低要从两个方面考虑:称量的溶质少了,量取的水多了进行分析;
(2)不能用水湿润pH试纸,否则稀释了待测溶液,使碳酸钠溶液的碱性减弱,据此进行分析解答;
(3)电解水时正极产生的气体是氧气;根据题意可知,氢氧化钠在电解水前后质量不变,那么可以求得其质量,然后再原溶液中溶质的质量分数为1%,求得原溶液的质量,进而得原溶液中水的质量.
解答 解:(1)①氢氧化钠既易潮解,又具有腐蚀性,不能放在纸上称量,要放在玻璃器皿中称量;
②A.a操作中砝码和氢氧化钠放错盘,会导致称量氢氧化钠质量偏小,会导致溶质质量分数偏低,故A正确;
B、b中烧杯用水洗涤后未干燥就使用,会导致水多了,也会使溶质质量分数偏低,故B正确;
C、应该需要水54mL,如果平视量筒凹液面最低处读数为50mL,水少了会导致溶质质量分数偏大,故C错;
D、d操作中有少量水溅出,水少了会导致溶质质量分数偏大,故D错;
故选AB;
(2)碳酸钠溶液显碱性,当溶液的pH大于7时,呈碱性,且pH越大,碱性越强;不能用水湿润pH试纸,否则稀释了待测溶液,使碳酸钠溶液的碱性减弱,测定结果偏小;
(3)电解水时正极产生的气体是氧气,用带火星的木条检验;由于电解掉的是水(加入少量氢氧化钠增强导电性),所以氢氧化钠质量不变,为100g×0.2%=0.2g,设电解掉水的质量为x,则$\frac{0.2g}{100g-x}$×100%=0.25%,解得x=20g,故被电解水的质量是20g.
故答案为:(1)①氢氧化钠直接放在纸上称量②AB
(2)偏小(3)带火星的木条;20
点评 易潮解或具有腐蚀性药品必须放在玻璃器皿中称量,导致溶质质量分数偏低要从两个方面考虑:称量的溶质和量取的水进行分析.

| A. | 桃木雕刻成桃木剑 | B. | 佛桃榨成汁 | ||
| C. | 佛桃腐烂 | D. | 桃花晒干泡茶 |
| A. | X的化学式是FeS2 | B. | FeS2是由铁元素和硫元素组成 | ||
| C. | 反应前后氧元素的化合价发生改变 | D. | SO2中的硫、氧元素的个数比为1:2 |
| A. |  过滤 | B. |  称量氢氧化钠 | C. |  稀释浓硫酸 | D. |  测定液体的pH |
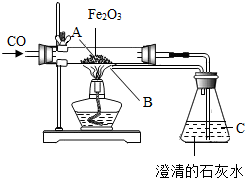 某课外活动小组的同学们在老师的帮助下,探究用赤铁矿(主要成分是Fe2O3)炼铁的主要反映原理.他们设计的实验装置如图所示,回答下列问题:
某课外活动小组的同学们在老师的帮助下,探究用赤铁矿(主要成分是Fe2O3)炼铁的主要反映原理.他们设计的实验装置如图所示,回答下列问题: