题目内容
某校化学研究小组对一种赤铁矿样品进行了研究,称取赤铁矿样品10g,把120g稀盐酸分四次加入样品中,测得实验数据见下表(假设赤铁矿中杂质不溶于水,也不与盐酸反应).
请回答:
(1)第4次剩余固体的质量m= ;
(2)该赤铁矿样品中氧化铁的质量分数为 ;
(3)计算所用稀盐酸的溶质质量分数.(写出必要的计算过程)
| 实验序号 | 第1次 | 第2次 | 第3次 | 第4次 |
| 加入稀盐酸质量/g | 30 | 30 | 30 | 30 |
| 剩余固体质量/g | 6.8 | 3.6 | 2 | m |
(1)第4次剩余固体的质量m=
(2)该赤铁矿样品中氧化铁的质量分数为
(3)计算所用稀盐酸的溶质质量分数.(写出必要的计算过程)
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)由于样品中除氧化铁外,其余的成分既不与盐酸反应,也不溶解于水,因此固体减少的质量为参加反应的氧化铁的质量,由表中每次加入30g稀盐酸固体减少的质量关系可判断:每加入30g稀盐酸固体应减少3.2g;据此规律,由第三次加入盐酸后固体质量的减少值小于3.2g可判断此次反应后碳酸钙已完全反应,剩余2g为杂质,第四次加入的盐酸未反应,m为杂志的质量2g;
(2)根据杂质的质量即可求出氧化铁的质量,进而求质量分数;
(3)由题意知,每加入30g稀盐酸固体减少3.2g,即30克盐酸能反应掉30克氧化铁,据此根据化学方程式进行计算.
(2)根据杂质的质量即可求出氧化铁的质量,进而求质量分数;
(3)由题意知,每加入30g稀盐酸固体减少3.2g,即30克盐酸能反应掉30克氧化铁,据此根据化学方程式进行计算.
解答:解:(1)每加入30g稀盐酸固体应减少3.2g;据此规律,由第三次加入盐酸后固体质量的减少值小于3.2g可判断此次反应后碳酸钙已完全反应,剩余2g为杂质,第四次加入的盐酸未反应,m为杂质的质量2g;
故答案为:2g;
(2)由题意知,杂质的质量为2克,所以赤铁矿样品中氧化铁的质量分数为:
×100%=80%;
故答案为:80%;
(3)设所用稀盐酸的溶质质量分数为x
Fe2O3+6HCl=2FeCl3+3H2O
160 219
3.2g 30×x
=
解得:x=14.6%
答:所用稀盐酸的溶质质量分数为14.6%.
故答案为:2g;
(2)由题意知,杂质的质量为2克,所以赤铁矿样品中氧化铁的质量分数为:
| 10g-2g |
| 10g |
故答案为:80%;
(3)设所用稀盐酸的溶质质量分数为x
Fe2O3+6HCl=2FeCl3+3H2O
160 219
3.2g 30×x
| 160 |
| 219 |
| 3.2g |
| 30×x |
解得:x=14.6%
答:所用稀盐酸的溶质质量分数为14.6%.
点评:学会正确分析图中数据是解题的关键.

练习册系列答案
相关题目
以下跟酒精灯有关的实验操作正确的是( )
A、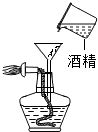 |
B、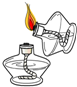 |
C、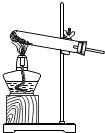 |
D、 |
给试管里的粉末物质加热时,以下操作不正确的是( )
| A、取用固体粉末未说明用量时,将固体粉末铺满试管底部即可 |
| B、使用试管夹时,手拿住试管夹的长柄 |
| C、加热时,试管必须与桌面成45度角倾斜 |
| D、加热的试管经冷却后再放到试管架上 |

 如图所示装置,有洗气、储气等多种用途.
如图所示装置,有洗气、储气等多种用途.