题目内容
4. 如图是探究金属活动性顺序的实验,A实验中的化学方程式为Cu+2AgNO3═Cu(NO3)2+2Ag.B实验中的现象为铝丝的表面有红色物质生成,溶液由蓝色逐渐变为无色.
如图是探究金属活动性顺序的实验,A实验中的化学方程式为Cu+2AgNO3═Cu(NO3)2+2Ag.B实验中的现象为铝丝的表面有红色物质生成,溶液由蓝色逐渐变为无色.
分析 在金属活动性顺序表中位于前面的金属能将后面的金属从其盐溶液中置换出来.根据发生的反应写出反应的化学方程式,回答反应的现象.
解答 解:由图示所示可知,将铜丝同时插入硝酸银溶液中,铜与硝酸银反应生成了银和硝酸铜,反应的化学方程式是:Cu+2AgNO3═Cu(NO3)2+2Ag;在B中铝与硫酸铜反应生成铜和硫酸铝,所以实验中的现象为:铝丝的表面有红色物质生成,溶液由蓝色逐渐变为无色.
故答为:Cu+2AgNO3═Cu(NO3)2+2Ag;铝丝的表面有红色物质生成,溶液由蓝色逐渐变为无色.
点评 本题的难度不大,了解金属活动性顺序及其应用是解答本题的基础知识.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
15.化学物质与人的生命活动息息相关,下列叙述中不正确的是( )
| A. | 二氧化碳是植物进行光合作用必需的物质 | |
| B. | 一氧化碳会与血液中的血红蛋白结合,使人中毒 | |
| C. | PM2.5是形成雾霾的主要元凶 | |
| D. | 房间内放一盆水,可防止一氧化碳中毒 |
12.分析推理是化学学习常用的方法,如表推理中不正确的是( )
| 选项 | 客观事实 | 推理 |
| A | 化合物是含有不同元素的纯净物 | 含不同种元素的纯净物一定是化合物 |
| B | NaOH固体溶于水放热 | Na+、OH-与水分子形成水合离子过 程中放出的热量大于Na+、OH-向水中扩散过程中吸收的热量 |
| C | 双氧水在常温下较难分解,而在加入二氧化锰后迅速分解 | 催化剂可加快反应速率 |
| D | 铜片在空气中很难燃烧,铜粉在空气中较易燃烧 | 反应物浓度影响反应进行的难易程度 |
| A. | A | B. | B | C. | C | D. | D |
16.下列化学方程式的书写和反应基本类型都正确的是( )
| A. | 赤铁矿冶炼生铁:3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 置换反应 | |
| B. | 石灰水检验二氧化碳:CO2+Ca(OH)2═CaCO3+H2O 复分解反应 | |
| C. | 电解水测定水的组成:2H2O═2H2↑+O2↑ 分解反应 | |
| D. | CO做燃料:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 化合反应 |
13.下列区分物质的方法中,不正确的是( )
| A. | 用闻气味的方法区分蒸馏水和酒精 | B. | 用点燃的方法区分甲烷和一氧化碳 | ||
| C. | 用肥皂水区分硬水和软水 | D. | 用石灰水区分氧气和二氧化碳 |
14.我们可以利用如下三种关系:对某些知识进行归纳,以对知识有更深刻的理解和认识,下列归纳和总结的关系,正确的是( )


| A. | 氧化反应和化合反应:交叉关系 | B. | 单质和氧化物:交叉关系 | ||
| C. | 化学反应和分解反应:并列关系 | D. | 混合物和冰水混合物:包含关系 |


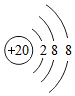 表示的粒子的符号是Ca2+;
表示的粒子的符号是Ca2+;