题目内容
 34、(本题有a、b两小题,考生任选一题解答,不得两题都解.若两题都解,则以 a小题计分)
34、(本题有a、b两小题,考生任选一题解答,不得两题都解.若两题都解,则以 a小题计分)我解答
a
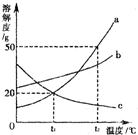
小题(请在横线上填写题号“a”或“b”以确认你的选择).a.如图是a、b、c三种物质(均不含结晶水)的溶解度曲线,请你回答:
(1)将tl℃时三种物质的饱和溶液升温至t2℃时,有晶体析出的是
c
;(2)t2℃时,将30g a物质加入到50g水中充分溶解,所形成溶液的质量是
75
g;(3)将t1℃时a、b、c三种物质的饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数大小关系是
b>a>c
.b.A、B两种物质的溶解度曲线如图.请你回答:
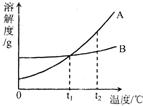
(1)在t2℃时,物质的溶解度B
小于
A(选填“大于”、“小于”或“等于”);(2)当B溶液中含有少量A时,可用
蒸发溶剂
法提纯B;(3)在t2℃时,一定量的A物质的饱和溶液蒸发掉10g水,可得到mgA晶体(不含结晶水),那么该温度时A的溶解度为
10m
g.(不要求计算过程)分析:理解固体溶解度的概念(在一定温度时,某固体物质在100克溶剂中达到饱和状态时所能溶解的质量)、溶解度曲线的意义及溶解度和温度之间的关系.
解答:解:a.(1)由于a和b的溶解度都随温度的升高而增大,而c的溶解度随温度的升高而减小,因此给三物质的饱和溶液升温时c的饱和溶液会有晶体析出,故选C
(2)由于在t2℃时,a的溶解度是50克,即在100克水中最多溶解50克a,在50克水最多溶解25克a,形成75克饱和溶液,故答案为:75
(3)由于在t1℃时,三物质的溶解度大小关系是:b>a═c,因此该温度下它们的饱和溶液中溶质的质量分数的大小关系是:b>a═c,若将t1℃时a、b、c三种物质的饱和溶液的温度升高到t2℃时,由于a和b的溶解度都随温度的升高而增大,因此升温时它们的饱和溶液就会变成不饱和溶液,但溶液中溶质的质量分数不变,而c的溶解度随温度的升高而减小,因此升温时它的饱和溶液就有晶体析出,导致溶液中溶质的质量分数减小,故选B>a>c
b.(1)由两物质的溶解度曲线不难看出在t2℃时,A的溶解度大于B的溶解度,故答案为:小于
(2)由于A的溶解度随温度的升高而增大,且受温度的影响大,而B的溶解度受温度的影响很小,因此当B溶液中含有少量A时,应采取蒸发溶剂的方法,故答案为:蒸发溶剂
(3)由于在t2℃时,一定量的A物质的饱和溶液蒸发掉10g水,可得到mgA晶体(不含结晶水),说明在10克水中最多溶解mgA,则100克水中就最多溶解10mgA,即在该温度下,A的溶解度是10mgA,故答案为:10m
(2)由于在t2℃时,a的溶解度是50克,即在100克水中最多溶解50克a,在50克水最多溶解25克a,形成75克饱和溶液,故答案为:75
(3)由于在t1℃时,三物质的溶解度大小关系是:b>a═c,因此该温度下它们的饱和溶液中溶质的质量分数的大小关系是:b>a═c,若将t1℃时a、b、c三种物质的饱和溶液的温度升高到t2℃时,由于a和b的溶解度都随温度的升高而增大,因此升温时它们的饱和溶液就会变成不饱和溶液,但溶液中溶质的质量分数不变,而c的溶解度随温度的升高而减小,因此升温时它的饱和溶液就有晶体析出,导致溶液中溶质的质量分数减小,故选B>a>c
b.(1)由两物质的溶解度曲线不难看出在t2℃时,A的溶解度大于B的溶解度,故答案为:小于
(2)由于A的溶解度随温度的升高而增大,且受温度的影响大,而B的溶解度受温度的影响很小,因此当B溶液中含有少量A时,应采取蒸发溶剂的方法,故答案为:蒸发溶剂
(3)由于在t2℃时,一定量的A物质的饱和溶液蒸发掉10g水,可得到mgA晶体(不含结晶水),说明在10克水中最多溶解mgA,则100克水中就最多溶解10mgA,即在该温度下,A的溶解度是10mgA,故答案为:10m
点评:主要考查对固体溶解度的概念的理解、溶解度曲线的意义及溶解度和温度间的关系,从而培养学生的理解能力和解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 33、(本题有a、b两小题,任选一题解答,不得两题都解.若两题都解,则以a小题记分)
33、(本题有a、b两小题,任选一题解答,不得两题都解.若两题都解,则以a小题记分)
 (本题有a、b两小题,考生任选一题解答,不得两题都解.若两题都解,则以a小题计分)
(本题有a、b两小题,考生任选一题解答,不得两题都解.若两题都解,则以a小题计分)