题目内容
7.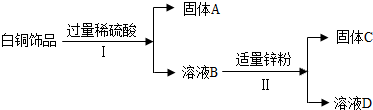 白铜(Cu、Ni合金)因为光泽好、耐腐蚀、容易加工等优点,常代替银做饰品.如图所示是某实验室分离废弃白铜饰品成分的流程(部分反应产物在图中已略去).
白铜(Cu、Ni合金)因为光泽好、耐腐蚀、容易加工等优点,常代替银做饰品.如图所示是某实验室分离废弃白铜饰品成分的流程(部分反应产物在图中已略去).已知溶液B中含有一种二价金属硫酸盐,溶液D中只有一种溶质.
分析该流程,回答下列问题:
(1)固体A的化学式为Cu,过程Ⅱ中的实验操作名称是过滤.
(2)过程Ⅰ中反应的化学方程式为Ni+H2SO4=NiSO4+H2↑.
(3)Cu、Ni、Zn的金属活动性由强到弱的顺序是Zn>Ni>Cu.
分析 根据金属能与酸反应的排在氢前面,不能与酸反应的排在氢的后面,活泼的金属能把不活泼的金属从盐溶液中置换出来分析金属活动性的顺序及反应过程中发生的反应并分析溶液中的成分.
解答 解:根据金属的活泼性顺序:铜在氢的后面与酸不反应,可知白铜饰品中加入过量的稀硫酸,镍可以与硫酸反应,已知溶液B中含有一种二价金属硫酸盐,故反应的化学方程式为:Ni+H2SO4=NiSO4+H2↑;溶液B为硫酸镍和稀硫酸的混合物,再加入适量的锌粉,因为溶液D中只有一种溶质.则是锌与硫酸反应生成硫酸锌和氢气,锌与硫酸镍反应生成硫酸锌和镍,说明锌比镍活泼.
(1)由以上分析可知:固体A的化学式为Cu,过程Ⅱ中的实验操作名称是过滤;
(2)过程Ⅰ中反应的化学方程式为Ni+H2SO4=NiSO4+H2↑;
(3)Cu、Ni、Zn的金属活动性由强到弱的顺序是Zn>Ni>Cu.
答案:
(1)Cu;过滤;
(2)Ni+H2SO4=NiSO4+H2↑;
(3)Zn>Ni>Cu
点评 此题以实验设计流程的形式让学生去利用金属活动性顺序表解决有关金属化学性质的问题,有一定的难度,解题的关键是熟练运用金属活动性的顺序意义.

练习册系列答案
相关题目
17.用浓盐酸配制一定溶质质量分数的稀盐酸,实验时必不可少的一组仪器是( )
| A. | 玻璃棒 量筒 烧杯 胶头滴管 | |
| B. | 托盘天平 量筒 烧杯 玻璃棒 | |
| C. | 托盘天平 玻璃棒 烧杯 胶头滴管 | |
| D. | 量筒 烧杯 漏斗 玻璃棒 |
18.甲和乙反应生成丙和丁的围观示意图如下,则下列说法中不正确的是( )
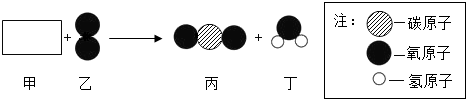

| A. | 甲物质的化学式为CH2O | |
| B. | 除甲以外其他物质都是氧化物 | |
| C. | 生成的丙、丁两物质的质量比是22:9 | |
| D. | 反应前后分子个数不变 |
15.某饮用水中含有较多的碳酸氢钙[Ca(HCO3)2],属于硬水,煮沸时会有水垢生成,实验小组欲探究该水垢的主要成分.
【猜想与分析】分析Ca(HCO3)2与水的元素组成,该水垢的主要成分可能是Ⅲ
Ⅰ;CaOⅡ.Ca(OH)2 Ⅲ.CaCO3 Ⅳ.Ca(OH)2和CaCO3
小强同学认为该水垢中不会存在CaO,理由是氧化钙能与水反应.
【实验与事实】
【原理与呈现】请用化学方程式表示实验二中有关反应的化学反应原理:CaCO3+2HCl═CaCl2+CO2↑+H2O,Ca(OH)2+CO2═CaCO3↓+H2O;
【实践与应用】使用硬水会给生活和生产带来许多麻烦,长期饮用硬水对人体健康不利,在日常生活中,可使用肥皂水来检测饮用水是硬水还是软水.
【猜想与分析】分析Ca(HCO3)2与水的元素组成,该水垢的主要成分可能是Ⅲ
Ⅰ;CaOⅡ.Ca(OH)2 Ⅲ.CaCO3 Ⅳ.Ca(OH)2和CaCO3
小强同学认为该水垢中不会存在CaO,理由是氧化钙能与水反应.
【实验与事实】
| 实验 | 现象 | 解释或结论 | |
| 实验一 | 将适量的水垢和水装入试管中,充分振荡后静置,用滴管取上层清液于小试管中,然后再向小试管中滴入紫色石蕊溶液 | 紫色石蕊溶液不变色 | Ca(OH)2微溶于水,其水溶液显碱性,能使紫色石蕊溶液变蓝色,不变色说明水垢中一定没有Ca(OH)2 |
| 实验二 | 按如图所示方案进行实验 | 反应一段时间后水垢消失,溶液澄清;玻璃片上澄清石灰水变浑浊 | 石灰水变浑浊,说明有CO2生成,则水垢中一定含有CaCO3 |
【实践与应用】使用硬水会给生活和生产带来许多麻烦,长期饮用硬水对人体健康不利,在日常生活中,可使用肥皂水来检测饮用水是硬水还是软水.
16.下列利用空气某成分物理性质的是( )
| A. | 氧气可以供给呼吸 | B. | 氮气可以制造化肥 | ||
| C. | 干冰用于人工降雨 | D. | 稀有气体用作保护气 |
 自行车是人们常用的交通工具,请根据如图回答下列问题.
自行车是人们常用的交通工具,请根据如图回答下列问题. 某学校兴趣小组在参与“五水共治”行动中,考察了某工厂的废水处理工程,并取该厂未经处理的废水样品进行测定分析:
某学校兴趣小组在参与“五水共治”行动中,考察了某工厂的废水处理工程,并取该厂未经处理的废水样品进行测定分析:
 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.