题目内容
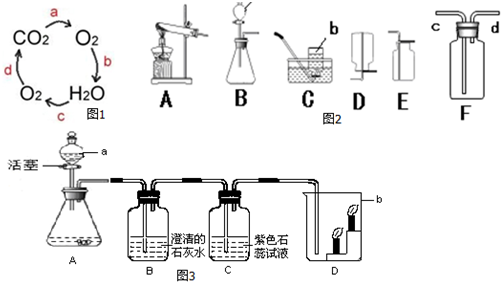
9.阅读下面科普短文(原文作者:袁越).二氧化碳是著名的温室气体,它能让太阳光顺利通过,却会阻止地表热量的散失.在地球形成的初期,太阳的辐射强度只有现在的四分之一,为什么那时的地球没有被冻成冰球呢?最新的理论认为,液态的水(比如降雨)能够溶解空气中的二氧化碳,再把它变为碳酸盐,沉积到岩石层中.同时,地球的内部很热,沉积在地壳中的碳经常会随着火山喷发而重新变为二氧化碳释放到大气中,这就形成了一个碳循环.经过几亿年的时间,这个碳循环逐渐达到了某种平衡,使大气中的二氧化碳保持一定的含量.正是由于这些二氧化碳产生的温室效应,使得地球的温度不至于太冷.
生命的诞生促成了另一个碳循环.众所周知,生命的基础是光合作用,就是利用太阳提供的能量,把二氧化碳中的碳元素提取出来,连接成一条长短不一的碳链.这样的碳链被称为“有机碳”,因为它既能作为生命的“建筑材料”,搭建成生命所需的各种有机分子(碳水化合物、蛋白质和氨基酸等),又能“燃烧自己”,产生能量供生命使用.有机碳的燃烧过程又可以称之为“氧化反应”,其产物就是二氧化碳和水.
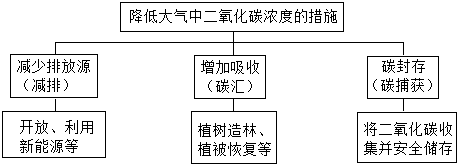
南极冰钻的结果证明,地球大气中的二氧化碳浓度在过去的1万年里基本保持稳定.但自工业化以来,由于化石燃料的大量使用,二氧化碳浓度开始逐年上升,同时段内地球大气层的平均温度也发生了变化.(见表一和表二)
目前燃烧化石能源而产生的二氧化碳,大气中的实际含量比理论计算值少一倍.有证据显示,大气中二氧化碳浓度的提高加快了森林的生长速度,促进了土壤对二氧化碳的吸收,这说明大自然正在努力地试图平衡人类带来的影响.但是,大自然的平衡能力是有限的,面对突然多出来的这些“碳”,大自然一时也应付不过来了,所以人类必须自己想办法.下图是当前人类为降低大气中的二氧化碳浓度所采取的措施.(有删改)
依据文章内容,回答下列问题.
(1)在地球形成的初期,地球没有被冻成冰球的原因是由于二氧化碳产生的温室效应,使得地球的温度不至于太冷.
(2)人类使用化石燃料使大气中二氧化碳浓度逐年上升.下列物质中,属于化石燃料的是ABD(填字母序号,下同).
A.天然气 B.煤 C.酒精 D.石油
(3)观察表一和表二后,小德认为二氧化碳排放量的持续增加导致地球大气层平均温度持续升高,但小威却不同意他的观点.下列不同年份间数据变化的总趋势能支持小威说法的是AC.
A.1900~1910 B.1910~1940 C.1940~1980 D.1980以后
(4)人类为降低大气中二氧化碳浓度采取的措施有:开发新能源、植树造林、碳封存(写出一条即可)等.
(5)关于碳循环,下列说法正确的是BC.
A.二氧化碳是温室气体,对人类的生活有害无利
B.保持自然界的碳循环处于平衡状态是至关重要的
C.人类过多的工业活动产生大量的二氧化碳,打破了碳循环的平衡
D.当碳循环的平衡状态被破坏时,大自然完全具有自我修复的能力.
分析 (1)根据题干信息结合二氧化碳是造成温室效应的气体之一来分析;
(2)天然气、煤、石油属于化石燃料;
(3)根据表格数据来分析;
(4)根据降低大气中二氧化碳含量的措施分析判断;
(5)根据二氧化碳的性质、用途及碳循环来分析.
解答 解:(1)有题干信息可知,二氧化碳产生的温室效应,使得地球的温度不至于太冷,所以在地球形成的初期,地球没有被冻成冰球;故填:由于二氧化碳产生的温室效应,使得地球的温度不至于太冷;
(2)化石燃料包括煤、石油和天然气,酒精不属于化石燃料;故填:ABD;
(3)1900~1910年二氧化碳的排放量增加,但是温度呈下降趋势;1940~1980年,二氧化碳的排放量迅速增大,但是温度变化不明显,二者均能支持小威说法;故填:AC;
(4)人类为降低大气中二氧化碳浓度采取的措施有:开发新能源、植树造林或将碳封存起来;故填:碳封存(答案合理);
(5)A.二氧化碳是绿色植物光合作用的原料,故错误;
B.保持自然界的碳循环处于平衡状态是至关重要的,故正确;
C.人类过多的工业活动产生大量的二氧化碳,打破了碳循环的平衡,故正确;
D.当碳循环的平衡状态被破坏时,大自然并不能完全自我修复,超过大自然自我修复的能力,就会引发自然灾害,故错误.
故填:BC.
点评 本题难度不大,了解温室效应的形成原因以及降低二氧化碳的方法等是正确解答本题的关键所在.

练习册系列答案
相关题目
4.下列图示与对应的叙述相符的是( )
| A. | 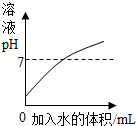 表示向稀盐酸中不断加水 表示向稀盐酸中不断加水 | |
| B. |  表示探究过氧化氢制氧气的反应中二氧化锰的作用 表示探究过氧化氢制氧气的反应中二氧化锰的作用 | |
| C. | 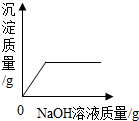 表示向盐酸和氯化镁的混合溶液中滴加氢氧化钠溶液 表示向盐酸和氯化镁的混合溶液中滴加氢氧化钠溶液 | |
| D. | 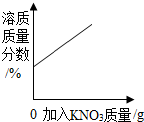 表示20℃时,向一定量的接近饱和的硝酸钾溶液中加入硝酸钾固体 表示20℃时,向一定量的接近饱和的硝酸钾溶液中加入硝酸钾固体 |
5.已知在相同的温度和压强下,相同体积的气体具有相同的分子数,20L天然气(CH4)充分燃烧消耗O2的体积可能是( )
| A. | 10L | B. | 15L | C. | 40L | D. | 50L |
17.实验室有一瓶长期存放的氢氧化钠固体,由于保管不当已经变质.某兴趣小组的同学欲通过实验测定其变质的情况.实验过程如下,取样品12.5g放入烧杯中,向其中加入140g过量的稀盐酸,充分反应后,得到148.1g溶液.
(1)试计算样品中碳酸钠的质量.
(2)实验后同学们做了认真的反思,一是普遍感受到合理保存药品的重要性,二是有同学觉得有必要验证一下所加140g稀盐酸是否过量,并征集了如下三个实验方案:
请助其完成实验报告,并选出其中在设计上不可行的方案,并简要说明理由:方案三不合理,因为NaCl与AgNO3反应也会产生白色沉淀,不能证明溶液中一定有HCl存在
还有细心的同学发现,上述实验在操作中也存在错误的地方,请帮他指出:方案一,将pH试纸浸入溶液中.
(1)试计算样品中碳酸钠的质量.
(2)实验后同学们做了认真的反思,一是普遍感受到合理保存药品的重要性,二是有同学觉得有必要验证一下所加140g稀盐酸是否过量,并征集了如下三个实验方案:
| 实验方案 | 一、测溶液pH | 二、滴加Na2CO3溶液 | 三、滴加AgNO3溶液 |
| 实验操作(先取适量实验后的废液与容器中) | 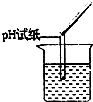 | 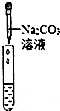 |  |
| 实验现象 | 试纸变色,对比比色卡:pH<7 | 有气泡冒出 | |
| 实验结论 | 稀盐酸已经过量 | ||
还有细心的同学发现,上述实验在操作中也存在错误的地方,请帮他指出:方案一,将pH试纸浸入溶液中.
18.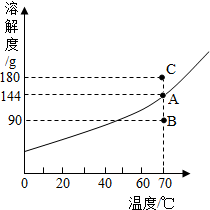 如图所示是固体KNO3的溶解度曲线,下列说法中正确的是( )
如图所示是固体KNO3的溶解度曲线,下列说法中正确的是( )
 如图所示是固体KNO3的溶解度曲线,下列说法中正确的是( )
如图所示是固体KNO3的溶解度曲线,下列说法中正确的是( )| A. | 70℃,KNO3的溶解度为144 | |
| B. | 70℃,A点对应溶液的溶质质量分数约为59% | |
| C. | 可通过升温的方法使B点处的溶液变为饱和溶液 | |
| D. | A、B、C三点对应溶液的溶质质量分数大小顺序依次为C>A>B |
19.分类法是化学学习和研究的重要方法之一.下列说法不正确的是( )
| A. | 空气、石油等都属于混合物 | |
| B. | KNO3、CO(NH2)2都属于复合肥料 | |
| C. | CH4、CH3COOH都属于有机化合物 | |
| D. | 锌、铁元素都属于人体必需的微量元素 |