题目内容
10.化学是一门以实验为基础的科学,请结合图示回答下列问题.
(1)用B装置在实验室里可制取O2(或CO2或H2)气体,写出制取气体的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑(或CaCO3+2HCl═CaCl2+H2O+CO2↑或Zn+H2SO4=ZnSO4+H2↑).
(2)用浓盐酸和石灰石在F中制取CO2并检验性质,观察到石蕊试液变红,变红的原因是二氧化碳气体与紫色石蕊试液的水反应生成碳酸,碳酸使紫色石蕊试液变红,化学方程式为CO2+H2O═H2CO3.
分析 (1)根据装置的特点来确定制取的气体并书写反应方程式;
(2)从石蕊试液是一种酸碱指示剂,它遇酸会变面红色,遇碱会变成蓝色.由于二氧化碳是氧化物不属于酸,不会使石蕊变红.“观察到石蕊试液变红”说明石蕊遇到了酸,说明是二氧化碳气体水反应生成碳酸去分析解答.
解答 解:(1)B装置适用于固液常温下来制取气体,如用大理石与稀盐酸反应制取二氧化碳,用锌粒与稀硫酸反应来制取氢气,用过氧化氢在二氧化锰的催化作用下来制取氧气,故填:O2(或CO2或H2);2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑(或CaCO3+2HCl═CaCl2+H2O+CO2↑或Zn+H2SO4=ZnSO4+H2↑)
(2)石蕊试液是一种酸碱指示剂,它遇酸会变面红色,遇碱会变成蓝色.由于二氧化碳是氧化物不属于酸,不会使石蕊变红.“观察到石蕊试液变红”说明石蕊遇到了酸,说明是二氧化碳气体与紫色石蕊试液的水反应生成碳酸,碳酸使紫色石蕊试液变红,其化学方程式为:CO2+H2O═H2CO3;故答案为:二氧化碳气体与紫色石蕊试液的水反应生成碳酸,碳酸使紫色石蕊试液变红;CO2+H2O═H2CO3.
点评 记住使石蕊试液变红不是二氧化碳气体而是二氧化碳和水反应生成的碳酸.

练习册系列答案
相关题目
8.下列除去物质中的少量杂质(括号内为杂质)的方法,错误的是( )
| A. | N2(O2)--通入足量的灼热铜网 | |
| B. | Ca(OH)2(CaO)--加入适量稀盐酸 | |
| C. | MnO2粉末 (KCl)--溶解、过滤、洗涤、干燥 | |
| D. | H2(水蒸气)--通过盛有足量浓硫酸的洗气瓶 |
1.比较、类推是学习中常用的思维方法.现有以下类推结果中正确的是( )
| A. | 碳酸钠、碳酸钙能与稀盐酸反应,所以所有的碳酸盐都可以与稀盐酸反应 | |
| B. | 碱的水溶液显碱性,所以碱性溶液一定是碱溶液 | |
| C. | 氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物 | |
| D. | 酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 |
5.下列各组中的物质混合,形成溶液的质量比反应前溶液的总质量减少的是( )
| A. | 氢氧化铜和稀硫酸 | B. | 氢氧化钠和稀盐酸 | ||
| C. | 氢氧化钙溶液和少量二氧化碳 | D. | 氢氧化钾和硝酸钠 |
15.用下列装置进行实验,不能达到实验目的是( )
| A. |  干燥 CO2 | B. |  收集 O2 | C. | 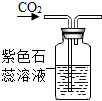 验证 CO2 性质 | D. |  监控气体流速 |
19.某同学对下列四个实验都设计了两种方案,其中两个方案都合理的是( )
| 选项 | A | B | C | D |
| 实验 目的 | 鉴别NaOH和 Na2CO3 | 除去NaOH溶液中少量的Na2CO3 | 除去氧化钙中的碳酸钙 | 除去氯化铁溶液中的盐酸 |
| 方案1 | 加水溶解,看是否放热 | 加适量Ca(OH)2溶液,过滤 | 高温煅烧 | 加过量铁粉,过滤 |
| 方案2 | 加入盐酸,看是否有气泡产生 | 加适量的氯化钙溶液,过滤 | 加适量稀盐酸,过滤 | 加过量氧化铁,过滤 |
| A. | A | B. | B | C. | C | D. | D |
20.根据下列实验目的,所选试剂及操作方法都正确的是( )
| 选项 | 实验目的 | 所选试剂及操作方法 |
| A | 除去二氧化碳中的少量一氧化碳气体 | 通入氧气、点燃 |
| B | 除去氯化钾中的二氧化锰 | 加水溶解、过滤、蒸发 |
| C | 除去氧化钙中的碳酸钙 | 加水溶解、过滤 |
| D | 除去稀盐酸中的稀硫酸 | 加入足量的氢氧化钡溶液、过滤 |
| A. | A | B. | B | C. | C | D. | D |
