题目内容
10.下列关于物质组成与分类的说法中正确的是( )| A. | 含有氧元素的化合物叫做氧化物 | |
| B. | 氢氧化钠的构成粒子是Na+和OH- | |
| C. | 原子核是由质子和电子构成的 | |
| D. | NH3由一个氮元素和三个氢元素组成 |
分析 根据氧化物的定义以及原子的构成,元素的定义等进行解答.
解答 解:A、氧化物是由两种元素组成,其中一种元素为氧元素,故含有氧元素的不一定是氧化物,例如KClO3故错误;
B、氢氧化钠的构成粒子是Na+和OH-,说法正确;
C、原子核是由质子与中子构成的,故C说法错误;
D、元素之间种类不讲个数,应该说NH3是由氮元素和氢元素组成的,故D说法错误;
故选B
点评 本题考查较为全面,注重基础,是一道基础题.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案
相关题目
10.下列做法中错误的是( )
| A. | 为减少白色污染,少使用塑料袋 | B. | 倡导低碳生活,多步行,少开车 | ||
| C. | 油锅着火时盖上锅盖灭火 | D. | 用氢氧化钠改良酸性土壤 |
15.硫酸铵和氯化钾是化工生产的副产品,直接作为肥料使用会使土壤酸化或影响作物的生长,工业上往往将氯化钾转化为无氯钾肥.如图1是硫酸铵等几种盐的溶解度曲线.回答下列问题:
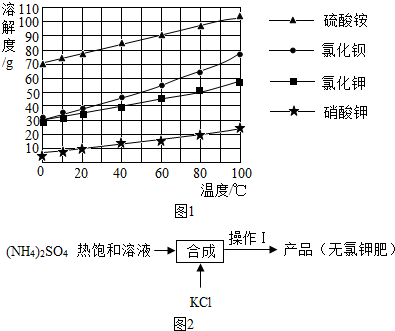
(1)根据溶解度曲线图,归纳硫酸铵等物质溶解度-温度曲线变化规律:
①硫酸铵等物质的溶解度,都是随温度升高而增大的;②温度相同时,各物质的溶解度不同.
(2)将氯化钾转化为无氯钾肥的流程如图2:
③根据溶解度曲线判断产品(无氯钾肥)的化学式是K2SO4;
④操作Ⅰ主要是趁热过滤,过滤后的产品中没有(NH4)2SO4晶体析出(填“有”或“没有”).
(3)苯甲酸(C6H5COOH)通常用作定香剂或防腐剂,也用作果汁饮料的保香剂,合成苯甲酸晶体常伴随有氯化钾等副产品生成,某同学加热分离氯化钾后的白色固体A,并测定其熔点,发现其在15℃开始熔化,达到130℃时仍有少量不熔.
资料:苯甲酸熔点122.4℃;纯净固体一般都有固定熔点;在常温时苯甲酸溶解度很小.小于0.4g.
【提出问题】分离氯化钾后的白色固体A的成分是什么?
【猜 想】猜想1:苯甲酸;猜想2:氯化钾,猜想3:苯甲酸和氯化钾的混合物.
【实验探究】限选试剂:蒸馏水、AgNO3溶液、稀硝酸.

(1)根据溶解度曲线图,归纳硫酸铵等物质溶解度-温度曲线变化规律:
①硫酸铵等物质的溶解度,都是随温度升高而增大的;②温度相同时,各物质的溶解度不同.
(2)将氯化钾转化为无氯钾肥的流程如图2:
③根据溶解度曲线判断产品(无氯钾肥)的化学式是K2SO4;
④操作Ⅰ主要是趁热过滤,过滤后的产品中没有(NH4)2SO4晶体析出(填“有”或“没有”).
(3)苯甲酸(C6H5COOH)通常用作定香剂或防腐剂,也用作果汁饮料的保香剂,合成苯甲酸晶体常伴随有氯化钾等副产品生成,某同学加热分离氯化钾后的白色固体A,并测定其熔点,发现其在15℃开始熔化,达到130℃时仍有少量不熔.
资料:苯甲酸熔点122.4℃;纯净固体一般都有固定熔点;在常温时苯甲酸溶解度很小.小于0.4g.
【提出问题】分离氯化钾后的白色固体A的成分是什么?
【猜 想】猜想1:苯甲酸;猜想2:氯化钾,猜想3:苯甲酸和氯化钾的混合物.
【实验探究】限选试剂:蒸馏水、AgNO3溶液、稀硝酸.
| 实验操作 | 实验现象 | 实验结论 |
| Ⅰ将白色固体A加入水中,加热、溶解、冷却、过滤. | 得到白色晶体和无色滤液 | |
| Ⅱ取无色滤液少许于试管中,滴加2-3滴硝酸银溶液 | 产生白色沉淀 | 白色固体A中含有KCl |
| Ⅲ取白色晶体,放入试管中加热 | 熔点是122.4℃ | 结合实验Ⅱ,猜想3成立 |
2.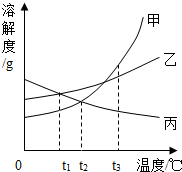 甲、乙、丙三种固体物质的溶解度曲线如图所示.下列叙述错误的是( )
甲、乙、丙三种固体物质的溶解度曲线如图所示.下列叙述错误的是( )
 甲、乙、丙三种固体物质的溶解度曲线如图所示.下列叙述错误的是( )
甲、乙、丙三种固体物质的溶解度曲线如图所示.下列叙述错误的是( )| A. | t1℃时,将等质量的甲、乙分别配成饱和溶液,所得溶液质量:甲>乙 | |
| B. | 将t1℃时甲、丙的饱和溶液升温到t2℃,两种溶液中溶质的质量分数相等 | |
| C. | 将t2℃时甲的饱和溶液变为t3℃时甲的饱和溶液,可以采用蒸发水的方法 | |
| D. | 将t3℃时三种物质的饱和溶液恒温蒸发等量水后,析出溶质的质量:甲>乙>丙 |
19.下列符号与其叙述对应一致的是( )
| A. | 3H-3个氢元素 | B. | C60-60个碳原子 | ||
| C. | $\stackrel{+3}{Fe}$-铁的化合价显+3价 | D. | NaCO-碳酸钠 |
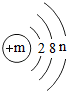 (其中n≠0),请回答下列问题.
(其中n≠0),请回答下列问题.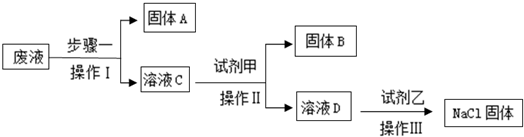
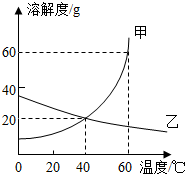 如图为甲、乙两种固体物质在水中的溶解度曲线,据此回答下列问题:
如图为甲、乙两种固体物质在水中的溶解度曲线,据此回答下列问题: