题目内容
13.下列物质中金属元素的质量分数最小的是( )| A. | Zn(NO3)2 | B. | Fe(NO3)3 | C. | NaNO3 | D. | Mg(NO3)2 |
分析 根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,根据硝酸盐的化学式,通过变形使硝酸根的个数相等,然后比较化合物中金属元素的原子的相对原子质量之和,金属元素原子的相对原子质量之和越大的,在硫酸盐中金属元素的质量分数就越大.
解答 解:在硝酸锌、硝酸铁、硝酸钠、硝酸镁四种物质中,将化学式变形得Zn(NO3)2、Fe$\frac{2}{3}$(NO3)2、Na2(NO3)2、Mg(NO3)2,因65>(23×2)>(56×$\frac{2}{3}$)>24,金属元素的原子相对原子质量之和越大的,在硫酸盐中金属元素的质量分数就越大,则金属元素的质量分数由小到大排列为Mg(NO3)2<Fe$\frac{2}{3}$(NO3)2<Na2(NO3)2<Zn(NO3)2.即Mg(NO3)2<Fe(NO3)3<NaNO3<Zn(NO3)2.
故选:D.
点评 本题考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力,据元素质量分数的计算方法将硫酸盐的化学式灵活变形是解答的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
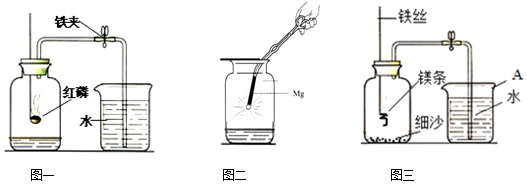
11.下列关于甲、乙、丙、丁四幅图的说法正确的是( )


| A. | 甲图:铝箔在氧气中剧烈燃烧,火星四射,放出热量,生成黑色固体 | |
| B. | 乙图:用火柴去点燃刚熄灭时的白烟,蜡烛能重新燃烧 | |
| C. | 丙图:小试管沿着大试管自动上升的原因可以用流速与压强的知识解释 | |
| D. | 丁图:钩码静止时,左右两弹簧测力计的读数不相同 |
1.ClO2是一种黄绿色、有刺激性气味的气体,在食品保鲜、饮用水消毒等方面有广泛应用.下列有关ClO2说法正确的是( )
| A. | 在物质分类上属于盐类 | B. | 具刺激性气味是一种物理性质 | ||
| C. | 相对分子质量为67.5克 | D. | 该物质中氯元素的化合价为+1价 |
18.下列实验操作或装置正确的是( )
| A. | 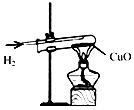 氢气还原氧化铜 氢气还原氧化铜 | B. | 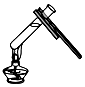 加热液体 | C. | 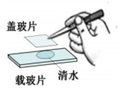 盖盖玻片 | D. |  使用测电笔 |
5.下列物质中一定属于混合物的是( )
| A. | 含氮35%的硝酸铵 | B. | 含铁70%的氧化铁 | C. | 冰和水的混合物 | D. | 含碳10%的碳酸钙 |
 .
. .
.