题目内容
8.杭州富春桃园景区的碧云洞内千姿百态的石笋、石柱的主要成分是碳酸钙.我校某科学兴趣小组为了测定石笋中碳酸钙的含量,取出了25克石笋放入盛有85克稀盐酸的烧杯中,但石笋完全反应后(杂质不与盐酸反应且不溶于水),称得烧杯内物质总质量为101.2克.(1)分析:由于该题中所涉及的三个数据均为混合物的数据,不能直接代入方程式进行计算,但是可以根据质量守恒定律,可算出二氧化碳的质量.
(2)计算所取石笋样品中碳酸钙的纯度.
分析 (1)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;根据题干内容分析得出反应前后的质量差即为生成二氧化碳气体的质量进行分析.
(2)根据反应的化学方程式,由放出二氧化碳的质量计算所取石笋样品中碳酸钙的质量.
解答 解:(1)根据质量守恒定律可知,生成二氧化碳的质量为:25g+85g-101.2g=8.8g.
(2)设所取石笋样品中碳酸钙的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 8.8g
$\frac{100}{x}=\frac{44}{8.8g}$
x=20g
所取石笋样品中碳酸钙的纯度=$\frac{20g}{25g}$×100%=80%
故答案为:
(1)质量守恒,二氧化碳;
(2)80%.
点评 利用质量守恒定律求出反应放出二氧化碳的质量,是进行后面计算的基础,体现出运用知识分析问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.用导管向盛有紫色石蕊试液的试管中吹气,过一会儿再给试管加热,则试管中溶液的颜色变化情况是( )
| A. | 紫色→红色→紫色 | B. | 紫色→蓝色→紫色 | C. | 紫色→红色→红色 | D. | 红色→紫色→红色 |
13.下列叙述中不正确的是( )
| A. | 严禁用一只燃着的酒精灯去点燃另一只酒精灯 | |
| B. | 严禁向燃着的酒精灯添加酒精 | |
| C. | 用过的药匙,可以用纸擦也可以不擦 | |
| D. | 倾倒液体时,瓶盖要倒放,标签要向着手心 |
17.下列关于氧气的说法中,错误的是( )
| A. | 氧气用于炼钢和医疗 | |
| B. | 氧气可以支持燃烧,说明氧气具有可燃性 | |
| C. | 氧气可以供给呼吸,是因为和体内物质反应而释放能量,维持生命活动 | |
| D. | 氧气不易溶于水,夏天鱼池内放增氧泵,增加氧气供给 |
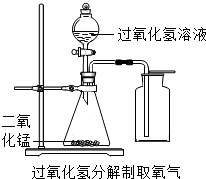 实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.
实验室中,常采用分解过氧化氢溶液(二氧化锰作催化剂)或加热高锰酸钾的方法制取氧气.