题目内容
6.某校化学兴趣小组的同学在学习了氧气的成份测定实验之后认为,测定氧气含量的方法有多种,他们也设计了一套实验装置,如图所示:实验前在一侧注射器内留有20mL的空气,然后给装有铜丝的硬质玻璃管加热,同时缓缓交替推拉两个注射器的活塞,至玻璃管内的铜丝变黑,且装置内的气体量不再进一步变化.停止加热,待冷却至室温后将气体全部推至一个注射器内.记录下注射器内的剩余气体的体积.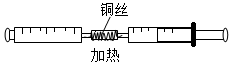
请根据你对上述实验的理解,回答下列问题:
(1)实验结束后,注射器内的气体理论上应该减少约4mL,这是因为空气中氧气约占总体积的1/5
(2)实验过程中,多次,缓慢交替推拉两个注射器的活塞的目的是让空气与铜丝充分接触,使注射器里的氧气能与铜丝充分反应
(3)如果该小组测得的空气中氧气含量大于理论值,可能的原因是点燃红磷后没有立即塞紧瓶塞
(4)如果该小组测得空气中氧气含量小于理论值,可能的原因是活塞不密封,注射器漏气
(5)如果氮气也能与铜反应,则该实验是否可行不可行.
分析 (1)铜丝与空气中的氧充分反应,消耗掉空气中氧气,由空气中氧气的体积比容易求出空气减少的体积.
(2)由实验条件可推出交替缓慢推动两个注射器的目的是使封闭空间的氧气充分反应.
(3)依据实验结果分析可能出现的情况即可;
(4)加入的铜丝的量必须是足量的,读数时应冷却至室温,装置的气密性必须好等.
(5)根据氮气与铜反应解答.
解答 解:(1)由于铜的氧化反应只消耗掉了空气中的氧气,而氧气在空气中约占空气体积的$\frac{1}{5}$,可得出答案:20mL×$\frac{1}{5}$=4mL;这是因为空气中氧气约占总体积的1/5;
(2)交替缓慢推动两个注射器的目的是使封闭空间的氧气与铜丝充分接触,使空气中的氧气与铜丝充分反应;
(3)点燃红磷后没有立即塞紧瓶塞,瓶内部分空气受热逸出,导致瓶内压强减小,水面上升高度超出,因此测出的空气中氧气的含量大于五分之一.
(4)改进后的实验只是粗略测定空气中氧气含量的一种方法,造成该实验不够精确的可能原因有以下几个原因:注射器的前端、玻璃管管比较细,不利于铜丝与注射器里的氧气反应,未交替缓缓推动两个注射器活塞,加入的铜丝量不足,没有完全消耗掉氧气,读数时没有冷却至室温等.点燃红磷后没有立即塞紧瓶塞,塞紧瓶塞之前,瓶内部分空气受热逸出,导致瓶内压强减小,水面上升高度超出,因此测出的空气中氧气的含量大于五分之一.
(5)如果氮气也能与铜反应,导致测量结果不准确,则该实验不可行.
答案:
(1)4,空气中氧气约占总体积的1/5;
(2)让空气与铜丝充分接触,使注射器里的氧气能与铜丝充分反应;
(3)点燃红磷后没有立即塞紧瓶塞;
(4)活塞不密封,注射器漏气;
(5)不可行
点评 本题能通过实验探究的方式考查了铜与氧气的反应,空气中氧的体积分数,提高了学生学以致用的意识.

 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | FeCl2 溶液(CuCl2) | 过量Fe粉 | 过滤 |
| B | Fe粉(Cu粉) | 适量稀盐酸 | 过滤 |
| C | Cu粉(Fe粉) | 水 | 过滤 干燥 |
| D | CO2(CO) | 足量O2 | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 燃着的木条 | B. | 灼热的氧化铜 | C. | 水 | D. | 澄清的石灰水 |
| A. | 硫 | B. | 铁 | C. | 镁 | D. | 碳 |
| A. | 清新的空气 | B. | 白酒 | C. | 食醋 | D. | 氧气 |
| A. | 建筑业上利用熟石灰制三合土或砌砖、抹墙 | |
| B. | 氢氧化钠可用于制肥皂和造纸业 | |
| C. | 实验室制得的二氧化碳常混有水蒸气,可以用氢氧化钠固体来除去 | |
| D. | 利用盐酸除去金属表面的锈 |
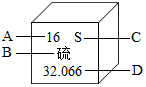 图是元素周期表中硫元素的信息示意图,对图中信息理解正确的是( )
图是元素周期表中硫元素的信息示意图,对图中信息理解正确的是( )| A. | 原子序数 | B. | 元素符号 | C. | 元素名称 | D. | 原子质量 |