题目内容
1. 如图,打开分液漏斗的活塞,让水滴入锥形瓶中(实验装置的气密性良好).立刻观察到(1)放热,液体沸腾,液滴飞溅;u型管中甲液面下降乙液面上升,用物理、化学知识解释产生以上现象的原因(2)水的密度较小,水会浮在浓硫酸的上面,溶解时放出的热能使水立刻沸腾,使硫酸液滴向四周飞溅,瓶内温度升高,瓶内气体压强增大,大于外界大气压,在压强的作用下,u型管中甲液面下降乙液面上升.
如图,打开分液漏斗的活塞,让水滴入锥形瓶中(实验装置的气密性良好).立刻观察到(1)放热,液体沸腾,液滴飞溅;u型管中甲液面下降乙液面上升,用物理、化学知识解释产生以上现象的原因(2)水的密度较小,水会浮在浓硫酸的上面,溶解时放出的热能使水立刻沸腾,使硫酸液滴向四周飞溅,瓶内温度升高,瓶内气体压强增大,大于外界大气压,在压强的作用下,u型管中甲液面下降乙液面上升.
分析 稀释浓硫酸时,必须把浓硫酸慢慢地倒入水中并不断搅拌.必须这样操作的原因是:浓硫酸溶于水放出大量的热,可以使水出现沸腾,若放出的热量不能及时扩散,将出现水受热不均匀而局部沸腾引起液体四处飞溅(爆沸);浓硫酸密度大于水,把浓硫酸倒入水中,硫酸会渐渐流动至底部,此过程也有利于热量的扩散.
解答 解:水密度小于浓硫酸,滴下的水滴浮于浓硫酸上;浓硫酸遇水放出大量的热,水立即沸腾,硫酸液滴飞溅,瓶壁上有小液滴,锥形瓶内压强增加,甲处水面下降,乙处水面上升.
故答案是:(1)放热,液体沸腾,液滴飞溅;u型管中甲液面下降乙液面上升;
(2)水的密度较小,水会浮在浓硫酸的上面,溶解时放出的热能使水立刻沸腾,使硫酸液滴向四周飞溅,瓶内温度升高,瓶内气体压强增大,大于外界大气压,在压强的作用下,u型管中甲液面下降乙液面上升.
点评 注意:在稀释浓硫酸时切不可把水倒入浓硫酸里,避免液体飞溅造成的伤害.

练习册系列答案
相关题目
5. 认识化学元素及化学符号是学习化学的重要内容,如表是人体和海水“大量元素”成分表:
认识化学元素及化学符号是学习化学的重要内容,如表是人体和海水“大量元素”成分表:
(1)在海水的大量元素中,含有的金属元素有4种
(2)用人体中含量前四位元素可以组成多种物质,请结合所学写出符合下列要求的物质各一种:①单质氧气,②氧化物水
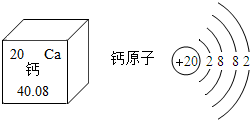
(3)如图所示,是钙元素在元素周期表中想相关信息.请回答:
①钙元素的原子序数是20
②钙原子易失(填“得”或“失”)电子,形成钙离子,钙离子的符号是Ca2+
③青少年缺钙易引起A(填序号)
A、佝偻病 B、贫血病 C、甲状腺肿大.
 认识化学元素及化学符号是学习化学的重要内容,如表是人体和海水“大量元素”成分表:
认识化学元素及化学符号是学习化学的重要内容,如表是人体和海水“大量元素”成分表:| 含量次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 人体中 | H | O | C | N | Na | Ca | P | S | K | Cl |
| 海水中 | H | O | Na | Cl | Mg | S | K | Ca | C | N |
(2)用人体中含量前四位元素可以组成多种物质,请结合所学写出符合下列要求的物质各一种:①单质氧气,②氧化物水
(3)如图所示,是钙元素在元素周期表中想相关信息.请回答:
①钙元素的原子序数是20
②钙原子易失(填“得”或“失”)电子,形成钙离子,钙离子的符号是Ca2+
③青少年缺钙易引起A(填序号)
A、佝偻病 B、贫血病 C、甲状腺肿大.
12.铝在一百多年里产量得到大幅度的提高,并被广泛地使用,原因之一就是铝的抗腐蚀性能好.铝具有良好抗腐蚀性能的原因是( )
| A. | 铝的化学性质不活泼 | |
| B. | 铝不与酸、氧气等物质反应 | |
| C. | 铝常温下不与氧气反应 | |
| D. | 铝表面形成一层致密的氧化铝保护膜 |
13.期末化学实验老师整理药品时,拿出一瓶久置的氢氧化钙粉末[Ca(OH)2],他让小王和大伟对这瓶氢氧化钙粉末的组成进行实验探究.
(1)提出问题:这瓶氢氧化钙是否已经生成碳酸钙(CaCO3)而变质?
(2)进行猜想:
①氢氧化钙全部变为碳酸钙;②氢氧化钙部分变为碳酸钙;③氢氧化钙没有变质.
(3)设计实验方案、进行实验:下表是对猜想①进行实验探究的过程示例:
请你另选择一种猜想参与探究,完成下表.
(4)原理与用途:
①氢氧化钙俗称熟石灰(或消石灰),其水溶液俗称石灰水,农业上一般采用氢氧化钙改良酸性土壤(选填“酸”或“碱”).
②氢氧化钙变质是由于与空气中的二氧化碳发生反应的缘故,反应的化学程式是:CO2+Ca(OH)2=CaCO3↓+H2O,因此氢氧化钙应密封保存.
(1)提出问题:这瓶氢氧化钙是否已经生成碳酸钙(CaCO3)而变质?
(2)进行猜想:
①氢氧化钙全部变为碳酸钙;②氢氧化钙部分变为碳酸钙;③氢氧化钙没有变质.
(3)设计实验方案、进行实验:下表是对猜想①进行实验探究的过程示例:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样,加适量水,搅拌,过滤 ①取少量滤液于试管中,滴入酚酞试液 ②取少量滤渣于试管中,加入盐酸 | ①滤液不变色 ②有气泡产生 | 氢氧化钙全部变 为碳酸钙 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取样,加适量水搅拌,过滤 ①取少量滤液于试管中,滴入酚酞试液 ②取少量滤渣于试管中,加入盐酸 | ① | |
| ② |
①氢氧化钙俗称熟石灰(或消石灰),其水溶液俗称石灰水,农业上一般采用氢氧化钙改良酸性土壤(选填“酸”或“碱”).
②氢氧化钙变质是由于与空气中的二氧化碳发生反应的缘故,反应的化学程式是:CO2+Ca(OH)2=CaCO3↓+H2O,因此氢氧化钙应密封保存.
10.正确的化学实验操作对实验结果、人身安全非常重要.下图中的实验操作正确的是( )
| A. | 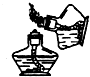 点燃酒精灯 | B. | 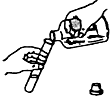 液体取用 | C. | 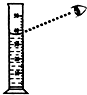 量取液体 | D. | 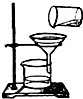 过滤 |
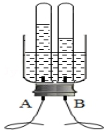 水是人类宝贵的自然资源,与人类的生产、生活密切相关.如图是电解水的装置图,请回答以下问题
水是人类宝贵的自然资源,与人类的生产、生活密切相关.如图是电解水的装置图,请回答以下问题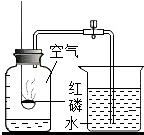 用来测空气成分的方法很多,如图所示的使用红磷在空气中燃烧的测定实验.实验过程是:将集气瓶容积等分五份,点燃燃烧匙里足量的红磷,伸入集气瓶中并把塞子塞紧,待红磷熄灭并冷却后,打开弹簧夹.
用来测空气成分的方法很多,如图所示的使用红磷在空气中燃烧的测定实验.实验过程是:将集气瓶容积等分五份,点燃燃烧匙里足量的红磷,伸入集气瓶中并把塞子塞紧,待红磷熄灭并冷却后,打开弹簧夹.