题目内容
3.一种白色固体A和黑色粉末B在加热条件下生成一种无色气体C.在C中,黄色粉末D剧烈燃烧,生成物色有刺激性气味的气体E.某常见金属F,在C中剧烈燃烧,火星四射,得黑色固体G.(1)物质A、G的名称分别是氯酸钾、四氧化三铁,物质B的作用是催化作用.
(2)无色气体C的相对分子质量是16.
(3)实验室完成反应D时,预先在集气瓶里装少量水的目的是吸收二氧化硫,防止空气污染.
(4)写出F在C中燃烧的化学方程式:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,此反应属于化合反应(基本类型).
分析 “在C中,黄色粉末D剧烈燃烧,生成无色有刺激性气味的气体E”为推断入口,得知C是氧气,D是硫磺,E是二氧化硫;然后通过F和氧气的反应现象推得F是铁G是四氧化三铁;进而推得A、B各是什么物质了
解答 解:依据“在C中,黄色粉末D剧烈燃烧,生成无色有刺激性气味的气体E”可知C是氧气,D是硫磺,E是二氧化硫;F和氧气的反应现象推得F是铁G是四氧化三铁;所以可根据白色固体A和黑色粉末B在加热条件下生成氧气,可知A是氯酸钾B是二氧化锰;
(1)由以上分析可知物质A、G的名称分别是氯酸钾,四氧化三铁; 物质B是氯酸钾分解制取氧气的催化剂,所起的作用是催化作用;
(2)根据题意知C是氧气,相对分子质量是16;
(3)二氧化硫是有毒气体,且能与水反应,所以实验室完成反应D时,预先在集气瓶里装少量水的目的是吸收二氧化硫,防止空气污染;
(4)铁丝在氧气中燃烧的反应表达式为铁+氧气 $\frac{\underline{\;点燃\;}}{\;}$四氧化三铁,该反应的反应物是两种生成物是一种,故该反应是化合反应;
故答案为:(1)氯酸钾,四氧化三铁; 催化作用;(2)16;(3)吸收二氧化硫,防止空气污染;(4)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;化合
点评 推断习题要善于根据习题中的信息来寻找突破口,抓住解决问题的关键,比如本题中的“在C中,黄色粉末D剧烈燃烧,生成无色有刺激性气味的气体E”既是解决此题的关键突破口.当然学生还得有过硬的基础知识根基

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
14.我市对生活垃圾已经实施分类投放,金属饮料罐应投放在标有哪种标志的垃圾箱中( )
| A. |  可回收废物 | B. |  有害垃圾 | C. |  厨房垃圾 | D. |  其它垃圾 |
18.下列反应属于中和反应的是( )
| A. | CaO+H2O═Ca(OH)2 | B. | CO2+2NaOH═Na2CO3+H2O | ||
| C. | Fe2O3+6HCl═2FeCl3+3H2O | D. | Mg(OH)2+2HCl═MgCl2+2H2O |
8.下列图象能正确反映对应变化关系的是( )
| A. |  足量红磷在密闭容器中燃烧 足量红磷在密闭容器中燃烧 | |
| B. |  将铜片加入一定量的硝酸银溶液中 将铜片加入一定量的硝酸银溶液中 | |
| C. |  向两份完全相同的稀盐酸中分别加入锌粉、镁粉 向两份完全相同的稀盐酸中分别加入锌粉、镁粉 | |
| D. |  向盛有一定量MnO2的烧杯中加入H2O2溶液 向盛有一定量MnO2的烧杯中加入H2O2溶液 |
15.某学习小组学习完碳的还原性后,对碳还原氧化铜后生成的气体是否一定是二氧化碳产生了怀疑.
【查阅资料】
①在本实验中为了保证实验成功,通过碳的质量是要过量的.
②被还原出来的铜在温度较高时很容易与空气中的氧气反应生成氧化铜.
③氮气不与碳、氧化铜产生反应,可用来隔绝空气(氧气).
【提出问题】木炭还原氧化铜产生的是什么气体?
根据质量守恒定律可知,产生的气体有三种情况
①全部是CO2 ②全部是CO ③一氧化碳与二氧化碳的混合物;
若猜想②成立,木炭还原氧化铜反应的化学方程式为:C+CuO$\frac{\underline{\;高温\;}}{\;}$CO↑+Cu.
【设计方案】由于二氧化碳可以被石灰水吸收面一氧化碳不能被石灰水吸收,从二氧化碳质量关系可以确定气体的组成.
【实验】
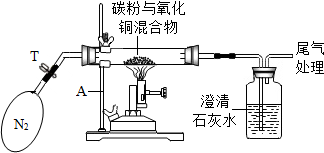
【结论】根据数据处理结果,得出猜想③成立.
【查阅资料】
①在本实验中为了保证实验成功,通过碳的质量是要过量的.
②被还原出来的铜在温度较高时很容易与空气中的氧气反应生成氧化铜.
③氮气不与碳、氧化铜产生反应,可用来隔绝空气(氧气).
【提出问题】木炭还原氧化铜产生的是什么气体?
根据质量守恒定律可知,产生的气体有三种情况
①全部是CO2 ②全部是CO ③一氧化碳与二氧化碳的混合物;
若猜想②成立,木炭还原氧化铜反应的化学方程式为:C+CuO$\frac{\underline{\;高温\;}}{\;}$CO↑+Cu.
【设计方案】由于二氧化碳可以被石灰水吸收面一氧化碳不能被石灰水吸收,从二氧化碳质量关系可以确定气体的组成.
【实验】

| 操作步骤及实验现象 | 简答 |
| ①称取0.8g氧化铜与0.2g碳粉均匀混合,放入重25g的玻璃管中,同时称得广口瓶和石灰水的总质量为500g,按图中装置连接 | / |
| ②加热前,先通一段时间纯净、干燥的氮气 | 其目的是 排走管内空气 |
| ③夹紧T处弹簧夹,加热一段时间,澄清石灰水变浑浊 | 澄清石灰水变浑浊的方程式为 CO2+Ca(OH)2═CaCO3↓+H2O |
| ④完全反应后,冷却至室温,称得玻璃管和固体总质量为25.66g | |
| ⑤称得广口瓶和石灰水的总质量为500.4g |
12.某化学活动小组开展了一次关于金属镉与铜、银活动性顺序的探究及水体镉污染事故处理方法的研讨.
【查阅资料】:①镉(Cd)是一种银白色金属,在化合物中通常表现为+2价;
②水体中镉元素通常以氯化镉的形式存在;
③氯化镉能溶于水、氢氧化镉难溶于水.
(1)金属镉与铜、银活动顺序的探究
实验结论:活动性顺序:镉>铜>银
(2)对镉污染事故处理方法的讨论.小华认为可用向受污染河段抛撒过量烧碱固体的方法除去氯化镉,反应的化学方程式表示为CdCl2+2NaOH═Cd(OH)2↓+2NaCl,小霞认为该方案虽然有效,但有缺陷,你认为可以用熟石灰(写化学式)代替烧碱.
【查阅资料】:①镉(Cd)是一种银白色金属,在化合物中通常表现为+2价;
②水体中镉元素通常以氯化镉的形式存在;
③氯化镉能溶于水、氢氧化镉难溶于水.
(1)金属镉与铜、银活动顺序的探究
| 实验步骤 | 实验现象 | 实验结论 |
| ①取适量镉、铜、银于试管中,加入足量 稀盐酸. | 镉表面有气泡产生,铜、银表面无气泡产生 | 镉的活动性顺序大于铜与银 |
| ② 取适量铜于试管中, 加入少量硝酸银溶液 | 铜表面覆盖了一层银白色物质, 溶液由无色变为蓝色. | 铜的活动性大于银.写出铜与硝酸银溶液反应的化学方程式: 铜的活动性顺序大于银 |
(2)对镉污染事故处理方法的讨论.小华认为可用向受污染河段抛撒过量烧碱固体的方法除去氯化镉,反应的化学方程式表示为CdCl2+2NaOH═Cd(OH)2↓+2NaCl,小霞认为该方案虽然有效,但有缺陷,你认为可以用熟石灰(写化学式)代替烧碱.
13..下列说法正确的是( )
| A. | 蒸馏水就是双氧水 | B. | 软水是不含钙镁化合物的水 | ||
| C. | 井水是硬水,雪水雨水是软水 | D. | 用肥皂水可以鉴别硬水和软水 |
 水是一种重要的资源.
水是一种重要的资源.