题目内容
19.如图是模拟海水制盐的流程图:
(1)操作X的名称是过滤;
(2)实验①加入过量Ca(OH)2溶液的目的是使氯化镁完全反应;
(3)写出实验②发生的其中一个反应Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;;
(4)写出实验④发生的中和反应NaOH+HCl═NaCl+H2O;
(5)精盐水中氯化钠的质量>粗盐水中氯化钠的质量.(填>、=、<)
分析 (1)根据过滤的原理分析;
(2)实验①加入过量Ca(OH)2溶液能使氯化镁完全反应;
(3)实验②中,碳酸钠和过量的氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,和氯化钙反应生成碳酸钙沉淀和氯化钠;
(4)实验④中,稀盐酸和碳酸钠反应生成生成氯化钠、水和二氧化碳,属于复分解反应,和氢氧化钠反应生成氯化钠和水,属于复分解反应或中和反应;
(5)精盐水中氯化钠的质量大于粗盐水中氯化钠的质量,这是因为反应过程中生成了氯化钠.
解答 解:(1)由操作过程可知,操作x能将固体和液体分开,名称是过滤;故填:过滤;
(2)实验①加入过量Ca(OH)2溶液能使氯化镁完全反应.故填:使氯化镁完全反应.
(3)实验②中,碳酸钠和过量的氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,和氯化钙反应生成碳酸钙沉淀和氯化钠,反应的化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH,Na2CO3+CaCl2═CaCO3↓+2NaCl.故填:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH; Na2CO3+CaCl2═CaCO3↓+2NaCl.
(4)实验④中,稀盐酸和碳酸钠反应生成生成氯化钠、水和二氧化碳,属于复分解反应,和氢氧化钠反应生成氯化钠和水,属于复分解反应或中和反应.故填:NaOH+HCl═NaCl+H2O.
(5)由于反应过程中生成了氯化钠,所以精盐水中氯化钠的质量大于粗盐水中氯化钠的质量.故填:>.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案
相关题目
7.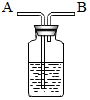 如图所示装置,有洗气、储气等用途,在医院给病人输氧气时,也利用了类似的装置,
如图所示装置,有洗气、储气等用途,在医院给病人输氧气时,也利用了类似的装置,
并在装置中盛放大约半瓶蒸馏水,以下说法中不正确的是( )
 如图所示装置,有洗气、储气等用途,在医院给病人输氧气时,也利用了类似的装置,
如图所示装置,有洗气、储气等用途,在医院给病人输氧气时,也利用了类似的装置,并在装置中盛放大约半瓶蒸馏水,以下说法中不正确的是( )
| A. | 该装置可以用来观察输出氧气的速度 | |
| B. | 该装置可用来观察是否已有氧气输出 | |
| C. | B导管连接病人吸氧气的塑料管 | |
| D. | B导管连接供给氧气的钢瓶 |
14.下列各组物质,能在 pH=1 的溶液中大量共存,且形成无色溶液的是( )
| A. | NaNO3、NaCl、CuSO4 | B. | NaOH、BaCl2、Na2SO4 | ||
| C. | NaCl、Na2SO4、Na2CO3 | D. | NaNO3、HCl、Na2SO4 |
4.对下列几种化学符号的说法不正确的是( )
①CH4既可以表示一种物质,又可以表示一个甲烷分子
②2H表示2个氢分子
③$\stackrel{+2}{Ca}$表示钙元素的化合价为+2价
④2Na+表示2个钠离子
⑤氧化铁的化学式为FeO.
①CH4既可以表示一种物质,又可以表示一个甲烷分子
②2H表示2个氢分子
③$\stackrel{+2}{Ca}$表示钙元素的化合价为+2价
④2Na+表示2个钠离子
⑤氧化铁的化学式为FeO.
| A. | ②⑤ | B. | ①③⑤ | C. | ①③④ | D. | ②④⑤ |
9.下列关于配制50g 10%的NaCl溶液的说法中,错误的是( )
| A. | 需称取NaCl 5g | |
| B. | 用50mL量筒量取45mL水 | |
| C. | 溶解时需要用玻璃棒搅拌 | |
| D. | 溶解时须把烧杯直接放在酒精灯上加热 |
 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
