题目内容
19.如图是实验室常用气体制备装置,据图回答问题:
(1)实验室用高锰酸钾制氧气的化学方程是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,应选择的收集装置是D(或F)(填字母代号).如果选用如图2装置收集氧气,气体应从a(填“a”或“b”)端导入.
(2)实验室用过氧化氢溶液和二氧化锰制氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.某化学小组同学用20%的过氧化氢溶液和二氧化锰,并选用B装置来制氧气.实验中,同学们发现不能得到平稳的氧气流.大家提出从两个方面加以改进:一是把发生装置由B改为C,其理由是可以控制液体流量来控制反应速率;二是将过氧化氢溶液加水稀释.溶液的稀释需要经过计算、量取、混匀等步骤.如果把50g质量分数为20%的过氧化氢溶液稀释成5%的过氧化氢溶液,需加水的质量为150g,在稀释过程中,除了烧杯外,还需要用到的仪器有①⑤⑥(填数字序号).
①量筒 ②药匙 ③试管 ④酒精灯 ⑤滴管 ⑥玻璃棒.
分析 (1)根据高锰酸钾制取氧气的原理写出反应的化学方程式,并据氧气的密度和溶解性确定收集装置,氧气密度比空气大,所以应从长管进气;
(2)根据实验室用过氧化氢溶液和二氧化锰制氧气的反应写出化学方程式;利用注射器加入液体时能控制加入液体的量;根据溶质质量不变原理计算加入水的质量,根据稀释的操作分析用到的玻璃仪器.
解答 解:(1)高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,反应的化学方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,因氧气的密度比空气大,不易溶于水,所以收集装置可选用D或F;如果选用图2装置收集氧气,气体应从长管进入,因为氧气的密度比空气大;
(2)实验室用过氧化氢溶液和二氧化锰制氧气的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,某化学小组同学用20%的过氧化氢溶液和二氧化锰,并选用B装置来制氧气.实验中,同学们发现不能得到平稳的氧气流.大家提出从两个方面加以改进:一是把发生装置由B改为C,原因是用注射器注入过氧化氢溶液,可以逐滴滴加液体,控制液体的流量,从而可控制产生氧气的速率;二是将过氧化氢溶液加水稀释.溶液的稀释需要经过计算需要的水的量、量筒量取液体、将要稀释的溶液与水混匀三个步骤.
如果把50g质量分数为20%的过氧化氢溶液稀释成5%的过氧化氢溶液,稀释过程中溶质的质量不变,设需加水的质量为为x,则50g×20%=(50g+x)×5%,解得 x=150g;在稀释过程中,除了烧杯外,还需要用到的仪器有:量取液体的量筒、定容用的滴管、用来搅拌的玻璃棒;
故答案为:(1)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;D(或F);a;
(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;可以控制液体流量来控制反应速率;量取、混匀;150;①⑤⑥.
点评 本题主要考查常用气体的发生装置和收集装置的选取方法以及注意事项、溶液的稀释的相关知识;并且要正确书写化学式和化学方程式;会利用题目中的信息处理问题.

 全优点练单元计划系列答案
全优点练单元计划系列答案| A. | 将垃圾分类回收利用 | B. | 远离烟草、拒绝毒品 | ||
| C. | 将工厂废渣直接排入江河 | D. | 改进燃煤技术,减少SO2与粉尘排放 |
| A. |  量取3.5mL液体 | B. |  甲烷验纯 | C. | 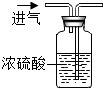 干燥二氧化碳 | D. |  测定溶液pH |
| A. | 目前氢能源没有广泛使用的主要原因是水资源严重不足 | |
| B. | 机动车轮胎和玻璃钢都是复合材料 | |
| C. | 塑料制品的回收再生,循环利用是减少白色污染的重要途径 | |
| D. | 有计划合理地开采金属矿产资源是保护金属资源的有效途径 |