题目内容
实验时用过氧化氢制取氧气,现取过氧化氢溶液50g,加入2.0g二氧化锰,充分反应后发生装置内剩余物的总质量为50.4g,求:
(1)生成氧气的质量.
(2)求该过过氧化氢溶液中溶质的质量分数,写出必要的计算过程.
(1)生成氧气的质量.
(2)求该过过氧化氢溶液中溶质的质量分数,写出必要的计算过程.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.故完全反应后称得剩余物质减少的质量就是生成气体的质量;
(2)根据过氧化氢分解反应的化学方程式和生成气体的质量,即可计算出实验中参加反应的过氧化氢的质量,进一步可求得过氧化氢溶液的质量分数.
(2)根据过氧化氢分解反应的化学方程式和生成气体的质量,即可计算出实验中参加反应的过氧化氢的质量,进一步可求得过氧化氢溶液的质量分数.
解答:解:(1)放出02的质量为:50g+2g-50.4g=1.6g
(2)设参加反应的过氧化氢的质量为x
2H2O2
2H2O+O2↑
68 32
x 1.6g
=
x=3.4g
过氯化氢溶液的质量分数为
×100%=6.8%
答:反应中放出02的质量为1.6 g,原过氧化氢溶液的质量分数为6.8%.
(2)设参加反应的过氧化氢的质量为x
2H2O2
| ||
68 32
x 1.6g
| 68 |
| 32 |
| x |
| 1.6g |
x=3.4g
过氯化氢溶液的质量分数为
| 3.4g |
| 50g |
答:反应中放出02的质量为1.6 g,原过氧化氢溶液的质量分数为6.8%.
点评:本题主要考查学生利用化学方程式进行计算的能力.

练习册系列答案
相关题目
建立宏观和微观之间的联系是化学学科特有的思维方式.下列对宏观事实的微观解释错误的是( )
| A、缉毒犬能根据气味发现毒品,是因为分子在不断地运动 |
| B、水蒸发为水蒸气,所占体积变大,是因为分子之间的间隔变大了 |
| C、10mL酒精和10mL水混合后体积小于20mL,是因为分子变小了 |
| D、不同的碱化学性质有所不同,是因为解离生成的金属阳离子不同 |
生活中一些常见物质的pH如图所示:
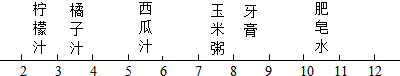
下列物质中,呈酸性的是( )

下列物质中,呈酸性的是( )
| A、西瓜汁 | B、牙膏 |
| C、肥皂水 | D、玉米粥 |
请利用你学过的化学知识判断下列物质的用途体现或利用物质物理性质的是( )
| A、用熟石灰改良酸性土壤 |
| B、用酒精给发烧病人降温 |
| C、用一氧化碳作还原剂炼铁 |
| D、用氧气急救病人 |
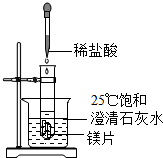 化学兴趣小组用如图装置进行实验,发现镁片完全溶解、石灰水浑浊.
化学兴趣小组用如图装置进行实验,发现镁片完全溶解、石灰水浑浊.