题目内容
5.实验室里同学们正在探究氢氧化钠与硫酸能否发生化学反应.【探究活动1】菲菲同学进行了如图1实验.
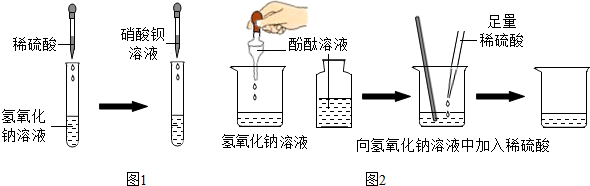
她观察到的现象应该是滴加稀硫酸后无现象,滴加硝酸钡溶液,产生白色沉淀.
她认为此现象说明生成了硫酸钠,因此能证明氢氧化钠与硫酸发生了反应.
【评价与交流】请你评价她的实验结论硫酸钠溶液中含有硫酸根离子,稀硫酸中也含有硫酸根离子,加入硝酸钡溶液产生硫酸钡白色沉淀,只能证明溶液中含有硫酸根离子,无法证明生成了其他物质.
【探究活动2】琪琪同学为了证明同样的问题进行了如图2的另一个实验:
【搜集证据】滴人酚酞后观察到溶液由无色变为红色,滴入适量稀硫酸后观察到溶液由红色变为无色.
【解释与结论】用化学方程式表示滴入稀硫酸后产生现象的原因H2SO4+2NaOH=Na2SO4+2H2O.
据此琪琪同学证明了氢氧化钠与硫酸能发生反应.
【反思与总结】由上述探究活动我们可以认识到,在判断一个反应能够发生时,如果不能证明有其它物质的生成,则应证明反应物发生了改变.
分析 【探究活动1】根据氢氧化钠溶液和硫酸反应生成硫酸钠和水,无现象解答;
【评价与交流】根据硫酸钠和硝酸钡,硫酸和硝酸钡都能产生硫酸钡白色沉淀解答;
【搜集证据】根据氢氧化钠溶液能够使酚酞变红,氢氧化钠和稀硫酸反应生成了硫酸钠和水,可以据此完成该题的解答;
【反思与总结】根据不能证明有其它物质的生成,则应证明反应物发生了改变解答.
解答 解:
【探究活动1】
氢氧化钠溶液和硫酸反应生成硫酸钠和水,无现象,滴加硝酸钡溶液,产生白色沉淀;
【评价与交流】
硫酸钠溶液中含有硫酸根离子,稀硫酸中也含有硫酸根离子,加入硝酸钡溶液产生硫酸钡白色沉淀,只能证明溶液中含有硫酸根离子,无法证明生成了其他物质;故不正确;
【搜集证据】氢氧化钠溶液能够使酚酞变红,所以在加入稀硫酸之前溶液呈红色,当加入稀硫酸,由于氢氧化钠和稀硫酸反应生成了硫酸钠和水,而硫酸钠为中性的溶液,所以可以观察到溶液的红色消失;
【解释与结论】氢氧化钠和硫酸反应生成硫酸钠和水,反应的方程式为:H2SO4+2NaOH=Na2SO4+2H2O;
【反思与总结】由上述探究活动我们可以认识到,在判断一个反应能够发生时,如果不能证明有其它物质的生成,则应证明反应物发生了改变;
答案:
【探究活动1】滴加稀硫酸后无现象,滴加硝酸钡溶液,产生白色沉淀
【评价与交流】硫酸钠溶液中含有硫酸根离子,稀硫酸中也含有硫酸根离子,加入硝酸钡溶液产生硫酸钡白色沉淀,只能证明溶液中含有硫酸根离子,无法证明生成了其他物质
【搜集证据】溶液由无色变为红色 溶液由红色变为无色
【解释与结论】H2SO4+2NaOH=Na2SO4+2H2O
【反思与总结】证明反应物发生了改变
点评 在做中和反应的实验时,由于酸和碱的溶液一般是无色,二者反应时的现象不明显,所以往往借助于一些试剂或仪器等(如酸碱指示剂、pH试纸、温度计等),来帮助我们判断反应是否进行或恰好完全.

 小学教材全测系列答案
小学教材全测系列答案| A | O2 | CO2 | H2O | |
| 反应前质量/g | 64 | a | 0 | 0 |
| 反应后质量/g | 0 | 0 | 88 | 72 |
(2)有机物A的相对分子质量为32.
 如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是( )
如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是( )| A. | 用蒸发甲或乙的溶液中的水的方法可以得到甲或乙的晶体 | |
| B. | t2℃时,甲的溶解度是110g | |
| C. | tl℃时,甲、乙的两种溶液溶质的质量分数相等 | |
| D. | t2℃时,用210 g甲的饱和溶液加水可以配制成550g 20%的甲溶液 |
| A. | 部分石蜡汽化 | B. | 棉线烛芯变黑 | ||
| C. | 蜡烛燃烧 | D. | 燃烧产物使澄清石灰水变浑浊 |
| A. | 汽油等可以挥发,说明分子可以不断运动 | |
| B. | 压瘪的乒乓球放入热水中重新鼓起来是因为分子体积增大 | |
| C. | 水分解生成氢气、氧气,说明分子可以破裂为原子 | |
| D. | 水和酒精能够互溶,说明分子之间有间隔 |
| A. | KNO3 NaOH NaNO3 | B. | K2CO3 KCl NaCl | ||
| C. | MgCl2 NaNO3 CuCl2 | D. | Ba(NO3)2 K2SO4 NH4NO3 |
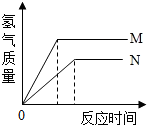 等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是A
等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是A