题目内容
11.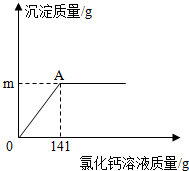 某纯碱样品中含有少量氯化钠,取该样品11g,全部溶液在100g水中,再逐渐滴加氯化钙溶液,反应的情况如图所示,A点时,过滤,得到滤液242g,计算:
某纯碱样品中含有少量氯化钠,取该样品11g,全部溶液在100g水中,再逐渐滴加氯化钙溶液,反应的情况如图所示,A点时,过滤,得到滤液242g,计算:(1)反应生成沉淀的质量m为10g.
(2)滤液中溶质的质量分数.
分析 碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠,反应物质量和滤液的质量差即为反应生成碳酸钙的质量,根据碳酸钙的质量可以计算碳酸钠的质量和生成的氯化钠的质量,进一步可以计算滤液中溶质的质量分数.
解答 解:(1)反应生成沉淀的质量为:11g+100g+141g-242g=10g,
故填:10.
(2)设碳酸钠的质量为x,生成氯化钠的质量为y,
Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 100 117
x 10g y
$\frac{106}{x}$=$\frac{100}{10g}$=$\frac{117}{y}$,
x=10.6g,y=11.7g,
滤液中溶质的质量分数为:$\frac{11g-10.6g+11.7g}{242g}$×100%=5%,
答:滤液中溶质的质量分数为:$\frac{11g-10.6g+11.7g}{242g}$×100%=5%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.锌元素的相关信息如图,下列有关锌的说法错误的是( )


| A. | 原子的核电荷数是30 | B. | 黄铜合金中通常含有锌元素 | ||
| C. | 锌不能置换稀硫酸中的氢 | D. | 相对原子质量为65.38 |
19.日常生活中发生下列变化,属于化学变化的是( )
| A. | 水果榨成汁 | B. | 木材劈成块 | C. | 高粱酿成酒 | D. | 小麦磨成面粉 |
6.推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 水能溶解许多种物质,因此水是一种溶液 | |
| B. | 物质燃烧需要同时满足三个条件,因此灭火也需要同时破坏这三个条件 | |
| C. | 碱溶液的pH>7,若测得某溶液的pH=12,因此该溶液一定是碱的溶液 | |
| D. | NaOH溶液中OH-能与酸反应,因此KOH溶液中的OH-也能与酸反应 |
16.下列是我市2015年基本实验操作考试中的部分操作,其中错误的是( )
| A. |  点燃酒精灯 | B. |  检查装置的气密性 | ||
| C. | 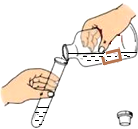 倾倒液体 | D. | 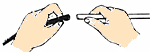 在玻璃管上套上胶皮管 |
3.某化合物是由氢、氧及另一种元素组成,下列对该化合物判断正确的是( )
| A. | 可能是盐 | B. | 可能是氧化物 | C. | 一定是碱 | D. | 不可能是酸 |
9.下列化学反应方程式和对应的反应类型都正确的是( )
| A. | NaOH+H2SO4═Na2SO4+H2O (复分解反应) | |
| B. | 4Fe+3O2 $\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 (化合反应) | |
| C. | H2O2$\frac{\underline{MnO_2}}{△}$H2↑+O2↑ (分解反应) | |
| D. | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ (置换反应) |
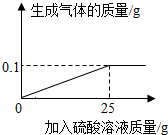 测定铁制品中铁的质量分数
测定铁制品中铁的质量分数