题目内容
17.中国科学家屠呦呦因创造性的研制出含青蒿素的抗疟新药,获得了2015年诺贝尔生理学或医学奖.青蒿素的化学式为C15H22O5,下列有关青蒿素的说法正确的是( )| A. | 青蒿素属于无机化合物 | |
| B. | 青蒿素分子的相对分子质量为282g | |
| C. | 青蒿素中碳、氢、氧三种元素的质量比为15:22:5 | |
| D. | 青蒿素中氢元素的质量分数为7.8% |
分析 A、根据含有碳元素的化合物叫有机化合物,简称有机物,进行分析判断.
B、相对分子质量单位是“1”,不是“克”,常常省略不写.
C、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
D、根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
解答 解:A、青蒿素是含碳元素的化合物,属于有机化合物,故选项说法错误.
B、相对分子质量单位是“1”,不是“克”,常常省略不写,故选项说法错误.
C、青蒿素中碳、氢、氧三种元素的质量比为(12×15):(1×22):(16×5)=90:11:40,故选项说法错误.
D、青蒿素中氢元素的质量分数为$\frac{1×22}{12×15+1×22+16×5}$×100%≈7.8%,故选项说法正确.
故选:D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
16.谚语诗词中蕴含着科学道理.下列说法正确的是( )
| A. | “真金不怕火炼”说明黄金熔点很高 | |
| B. | “满架蔷薇一院香”说明分子在不停地运动 | |
| C. | “百炼成钢”与“只要功夫深铁杵磨成针”蕴含的化学原理相同 | |
| D. | “众人拾柴火焰高”是指可燃物越多,着火点越低,越容易着火 |
2.碳酸钡广泛应用于显像管(CRT)、陶瓷、光学玻璃等行业.有一种碳酸盐矿石其主要成分为碳酸钡和碳酸钙,以此矿石为原料生产碳酸钡的流程如图所示.
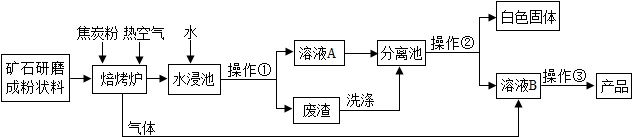
已知:碳酸钡和碳酸钙具有相似的化学性质,高温下能分解成两种氧化物;氧化钡和氧化钙都能与水反应生成对应的氢氧化物,这两种氢氧化物均可以和二氧化碳反应.但氢氧化物溶解度有一定的差异,下表所示的是两种氢氧化物在不同温度下的溶解度.
(1)写出焙烧炉中含钡元素物质发生反应的化学方程式:BaCO3$\frac{\underline{\;高温\;}}{\;}$BaO+CO2↑
(2)除了水之外,进入分离池中的物质是氢氧化钡和氢氧化钙,请你推测分离池中操作②的方法是B(选填“A”或“B”).
A.降温,过滤;B.加热,过滤
(3)写出由溶液B制取产品的化学方程式:Ba(OH)2+CO2=BaCO3↓+H2O
(4)以下相关说法正确的是ABD.
A.对矿石进行预处理“研磨成粉状”有利于充分反应
B.焙烧炉中添加焦炭粉和热空气是为了维持炉内的高温状态
C.焙烧炉内只涉及分解反应
D.废渣需要经过洗涤才能弃渣,是为了保护环境,同时充分利用原料.

已知:碳酸钡和碳酸钙具有相似的化学性质,高温下能分解成两种氧化物;氧化钡和氧化钙都能与水反应生成对应的氢氧化物,这两种氢氧化物均可以和二氧化碳反应.但氢氧化物溶解度有一定的差异,下表所示的是两种氢氧化物在不同温度下的溶解度.
| 温度/℃ | 0 | 40 | 80 |
| Ca(OH)2溶解度/g | 0.187 | 0.141 | 0.094 |
| Ba(OH)2溶解度/g | 1.67 | 8.22 | 101.4 |
(2)除了水之外,进入分离池中的物质是氢氧化钡和氢氧化钙,请你推测分离池中操作②的方法是B(选填“A”或“B”).
A.降温,过滤;B.加热,过滤
(3)写出由溶液B制取产品的化学方程式:Ba(OH)2+CO2=BaCO3↓+H2O
(4)以下相关说法正确的是ABD.
A.对矿石进行预处理“研磨成粉状”有利于充分反应
B.焙烧炉中添加焦炭粉和热空气是为了维持炉内的高温状态
C.焙烧炉内只涉及分解反应
D.废渣需要经过洗涤才能弃渣,是为了保护环境,同时充分利用原料.
6.在四个烧杯中都放入Na2CO3和NaCl固体混合物24.8g,分别加入盐酸进行四次实验,所加盐酸和反应后溶液的质量如下表所示:
(1)四个实验中恰好完全反应的是实验二
(2)计算完全反应的实验中所得溶液中溶质的质量分数(CO2的溶解忽略不计).
| 实验序数 | 实验一 | 实验二 | 实验三 | 实验四 |
| 所加盐酸的质量 | 316g | 326g | 336g | 346g |
| 反应后溶液的质量 | 334.5g | 342g | 352g | 362g |
(2)计算完全反应的实验中所得溶液中溶质的质量分数(CO2的溶解忽略不计).
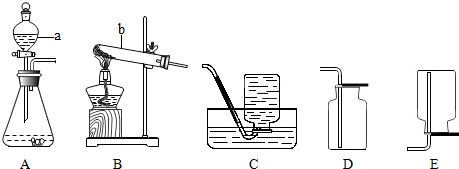
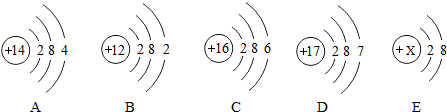
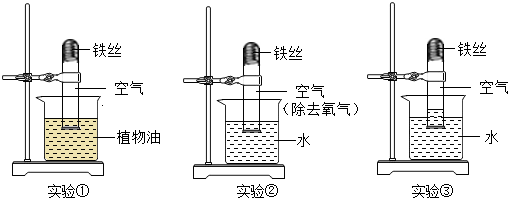
 纯碱是一种重要的化工原料,广泛应用于玻璃、造纸、纺织和洗涤剂的生产.
纯碱是一种重要的化工原料,广泛应用于玻璃、造纸、纺织和洗涤剂的生产. 所示.该气体遇空气中的水蒸气易形成酸雾,腐蚀金属设备.该酸雾腐蚀金属铁的化学方程式为Fe+2HCl═FeCl2+H2↑.
所示.该气体遇空气中的水蒸气易形成酸雾,腐蚀金属设备.该酸雾腐蚀金属铁的化学方程式为Fe+2HCl═FeCl2+H2↑.