题目内容
1.如图表示自来水消毒过程中发生反应的微观过程.下列叙述正确的是( )
| A. | 该反应是置换反应 | |
| B. | 反应前后原子的种类和数目不变 | |
| C. | 反应可表示为:2H2O+Cl2=HCl+HClO+H2O | |
| D. | 反应前后元素化合价均无变化 |
分析 根据图示,结合质量守恒定律进行分析,图中是一种单质和一种化合物生成了两种化合物.据此解答即可.
解答 解:题目中图变为: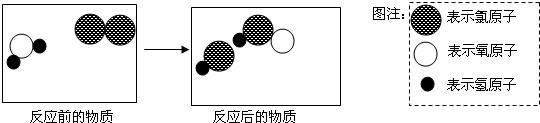
A、图中是一种单质和一种化合物生成了两种化合物,故A错误;
B、化学反应前后,元素的种类和原子的种类和个数不变,故B正确;
C、图中反应可表示为:H2O+Cl2=HCl+HClO,故C错误;
D、据图可知,水与氯气反应生成氯化氢和偏氯酸,则可推测反应前后元素化合价有变化,故D错误;
故选B.
点评 本题考查了化学反应实质用微观模型示意图表示,完成此题,可以依据化学反应的实质结合质量守恒定律进行.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
11.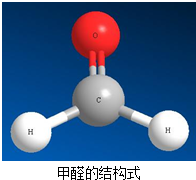 甲醛(HCHO)是一种无色,有强烈刺激性气味的气体,具有致癌性、属于高毒物,易溶于水,35%~40%的甲醛水溶液叫福尔马林.下列有关甲醛的说法正确的是( )
甲醛(HCHO)是一种无色,有强烈刺激性气味的气体,具有致癌性、属于高毒物,易溶于水,35%~40%的甲醛水溶液叫福尔马林.下列有关甲醛的说法正确的是( )
 甲醛(HCHO)是一种无色,有强烈刺激性气味的气体,具有致癌性、属于高毒物,易溶于水,35%~40%的甲醛水溶液叫福尔马林.下列有关甲醛的说法正确的是( )
甲醛(HCHO)是一种无色,有强烈刺激性气味的气体,具有致癌性、属于高毒物,易溶于水,35%~40%的甲醛水溶液叫福尔马林.下列有关甲醛的说法正确的是( )| A. | 甲醛中碳、氢、氧原子的个数比为1:2:1 | |
| B. | 甲醛分子中碳、氧元素的质量比为3:4 | |
| C. | 甲醛是由多原子分子构成的有机高分子化合物 | |
| D. | 1个甲醛分子中的质子和电子数目相等,均为14个 |
12.下列有关化学知识的说法中,不正确的是( )
| A. | 活性炭具有吸附性,可以用来净化水 | |
| B. | CO、C具有还原性,常用来冶炼金属 | |
| C. | 胃液中少量的盐酸,可以帮助消化 | |
| D. | 人体代谢产生的CO2,如不能及时排出会使血液的pH增大 |
6.如表是NaOH和Ca(OH)2的溶解度数据,请回答下列问题.
(1)从表中数据可以获得的信息是Ca(OH)2的溶解度随温度的升高而减小(写一条);
(2)在保持溶质质量分数不变的情况下,将NaOH的不饱和溶液变成饱和溶液的方法是降温;
(3)实验室要配制溶质质量分数较大的饱和石灰水,应使用冷水(填“冷水”或“热水”)进行实验.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaOH | 31 | 91 | 111 | 129 | 313 | 336 |
| Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | |
(2)在保持溶质质量分数不变的情况下,将NaOH的不饱和溶液变成饱和溶液的方法是降温;
(3)实验室要配制溶质质量分数较大的饱和石灰水,应使用冷水(填“冷水”或“热水”)进行实验.
10.下列实验设计,不能达到实验目的是( )
| 选项 | 实验目的 | 实验设计 |
| A | 鉴别蒸馏水与氯化钾溶液 | 取样后,加热蒸发 |
| B | 检验废水中是否含有Cl- | 取样后,滴加AgNO3溶液和稀硝酸 |
| C | 鉴别硬水和软水 | 取样后,分别加入肥皂水,振荡 |
| D | 除去CO2中的CO | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
11.下列实验操作或设计中正确的是( )
| A. | 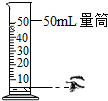 量取 8.5mL 盐酸 | B. |  证明不同物质的着火点不同 | ||
| C. |  分离碘酒中的碘 | D. |  验证质量守恒定律 |
