题目内容
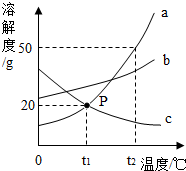 如图是a、b、c三种固体物质的溶解度曲线.
如图是a、b、c三种固体物质的溶解度曲线.(1)由图中 信息可知:P点表示的意义:
(2)要使接近饱和的c物质的溶液变为饱和溶液,可采取的一种措施是
(3)现有t2℃时的a、b、c三种物质的饱和溶液,将其都降温至t1℃时,析出溶质最多的是
(4)t2℃时,将60克a物质放入100克水中,充分搅拌,所得溶液的质量
(5)计算P点(t1℃时)a、c两物质饱和溶液的溶质质量分数为
考点:固体溶解度曲线及其作用,饱和溶液和不饱和溶液相互转变的方法,晶体和结晶的概念与现象,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)溶解度曲线的交点表示该温度下两物质的溶解度相等;据物质的溶解度可知物质的溶解度随温度变化情况;
据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(2)不饱和溶液变为饱和溶液的一般方法是加入溶质、蒸发溶剂、降温,据此分析解答;
(3)等质量的饱和溶液降低相同的温度,溶解度变化大的析出溶质多;
(4)据该温度下a的溶解度分析判断;
(5)据饱和溶液中溶质的质量分数计算方法分析解答.
据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(2)不饱和溶液变为饱和溶液的一般方法是加入溶质、蒸发溶剂、降温,据此分析解答;
(3)等质量的饱和溶液降低相同的温度,溶解度变化大的析出溶质多;
(4)据该温度下a的溶解度分析判断;
(5)据饱和溶液中溶质的质量分数计算方法分析解答.
解答:解:(1)由图中 信息可知:P点是t1℃时ac的溶解度曲线的交点,二者的溶解度相等;由线C可知:c的溶解度随温度升高而减小;
(2)c的溶解度随温度升高而减小,所以要使接近饱和的C物质的溶液变为饱和溶液,可采取加入溶质、蒸发溶剂、升温的方法;
(3)现有t2℃时的a、b、c三种物质的饱和溶液,将其都降温至t1℃时,a的溶解度变化比b大,析出溶质最多,c溶解度变大,不会析出晶体;
(4)t2℃时a的溶解度是50g,所以将60克a物质放入100克水中,充分搅拌,最多溶解50g的a,所得溶液的质量150 克;
(5)饱和溶液中溶质的质量分数=
×100%,P点(t1℃时)a、c两物质的溶解度是20g,所以饱和溶液的溶质质量分数为
×100%≈16.7%;
故答案为:(1)t1℃时ac的溶解度相等;c的溶解度随温度升高而减小;
(2)加入c物质(合理均可);
(3)a;
(4)150;
(5)16.7%.
(2)c的溶解度随温度升高而减小,所以要使接近饱和的C物质的溶液变为饱和溶液,可采取加入溶质、蒸发溶剂、升温的方法;
(3)现有t2℃时的a、b、c三种物质的饱和溶液,将其都降温至t1℃时,a的溶解度变化比b大,析出溶质最多,c溶解度变大,不会析出晶体;
(4)t2℃时a的溶解度是50g,所以将60克a物质放入100克水中,充分搅拌,最多溶解50g的a,所得溶液的质量150 克;
(5)饱和溶液中溶质的质量分数=
| 溶解度 |
| 溶解度+100g |
| 20g |
| 120g |
故答案为:(1)t1℃时ac的溶解度相等;c的溶解度随温度升高而减小;
(2)加入c物质(合理均可);
(3)a;
(4)150;
(5)16.7%.
点评:了解溶解度曲线的意义、溶解度概念、饱和溶液中溶质的质量分数等知识,即可结合题意灵活分析解答.

练习册系列答案
相关题目
下列物质的应用正确的是( )
A、 钛合金制钢轨 |
B、 氢氧化钙制干燥剂 |
C、 氮气用于制氮肥 |
D、 碳酸钠用于铅蓄电池 |
 把等质量的X、Y、Z、M四种金属分别加入到同体积、同浓度的足量稀盐酸中.再把M加入到YNO3溶液中.反应关系如图所示.据此判断四种金属的活动性顺序为( )
把等质量的X、Y、Z、M四种金属分别加入到同体积、同浓度的足量稀盐酸中.再把M加入到YNO3溶液中.反应关系如图所示.据此判断四种金属的活动性顺序为( )| A、Z>X>M>Y |
| B、X>Z>M>Y |
| C、X>Z>Y>M |
| D、Y>M>Z>X |


