题目内容
1.甲、乙两同学利用下面装置测定铜和氧化铜的混合物中铜元素的质量分数.回答问题: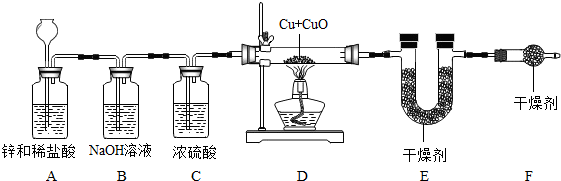
①A中发生的化学方程式Zn+2HCl═ZnCl2+H2↑.
②B装置作用除去氢气中的HCl.
③D装置中铜和氧化铜总质量为10克,充分反应后,欲求原混合物中铜元素的质量分数,还需要的实验数据是E装置增加的质量(或D装置中剩余固体的质量).
④F装置的作用是吸收空气中的水,如果没有F装置,会使实验结果偏小(偏大、偏小).
分析 ①根据锌和盐酸生成氯化锌和氢气进行解答;
②根据盐酸具有挥发性进行解答;
③根据E装置增加的质量为水的质量进行解答;
④根据如不加F装置会使得空气中水蒸气进入使得水的质量增加,那么计算出的氧化铜的质量也随着增加,所以会使实验结果偏小进行解答
解答 解:①锌和盐酸生成氯化锌和氢气,A中可观察到的现象为Zn粒逐渐减少,且有气泡产生;反应的化学方程式为:Zn+2HCl═ZnCl2+H2↑;
②盐酸具有挥发性,挥发出氯化氢气体,氢氧化钠和氯化氢反应生成氯化钠和水,所以B装置的作用是除去氢气中的HCl;
③欲求原混合物中铜元素的质量分数,除了要知道原混合物总质量外还需要知道E装置增加的质量,即为生成水的质量,根据生成水的质量计算氧化铜的质量.或知道D装置中剩余固体的质量,即铜元素的质量.
④如不加F装置会使得空气中水蒸气进入使得水的质量增加,那么计算出的氧化铜的质量也随着增加,所以会使实验结果偏小.
故答案为:①Zn+2HCl═ZnCl2+H2↑;
②除去氢气中的HCl;③E装置增加的质量(或D装置中剩余固体的质量);④偏小.
点评 该题是一道综合实验题,实验设计严密,考查的知识点较多,解题的关键是明确实验目的和原理,分析综合装置各部分的作用.

练习册系列答案
相关题目
12.京京在做金属与盐溶液的实验时,意外发现铝放入硫酸铜溶液后产生了无色无味气体,于是对此进行探究.
【提出猜想】①欢欢认为该气体可能是氧气②迎迎认为该气体可能是氢气③晶晶认为该气体可能是二氧化硫.欢欢认为晶晶的猜想错误,理由是二氧化硫是一种有刺激性气味的气体.
【进行探究】
【反思与探究】铝为什么能与硫酸铜溶液反应产生该气体?京京思考除与水有关外,还与什么粒子有关呢?资料表明硫酸铜在水中会产生铜离子和硫酸根离子.为此京京又进行以下实验:
由上述实验可以推出,硫酸铜溶液中可能含有酸性物质.
【提出猜想】①欢欢认为该气体可能是氧气②迎迎认为该气体可能是氢气③晶晶认为该气体可能是二氧化硫.欢欢认为晶晶的猜想错误,理由是二氧化硫是一种有刺激性气味的气体.
【进行探究】
| 实验操作 | 实验现象 | 结论 |
| ①先用试管收集该气体,再将带火星的木条伸入试管 | 木条不复燃 | 欢欢猜想不成立 |
| ②用尖嘴导管将气体导出并引燃,同 时在上方放一块干冷的玻璃片 | 气体燃烧,产生蓝色火焰且玻璃片上有水雾出现 | 迎迎猜想成立 |
| 实验操作 | 实验现象 | 实验结论 |
| 把铝丝放入20%的硫酸钠溶液 | 无气泡产生 | 产生该气体与硫酸根离子无关 |
| 把铝丝放入20%的CuSO4溶液 | 有气泡产生 | 产生气泡与铜离子有关 |
9.下列实验操作示意图正确的是( )
| A. | 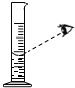 量取液体时读数 | B. |  稀释浓硫酸 | ||
| C. |  过滤 | D. | 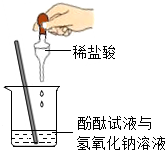 酸碱中和 |
16.下列变化中,前者属于物理变化后者属于化学变化的是( )
| A. | 火药爆炸、氢氧化钠潮解 | B. | 活性炭净水、浓盐酸挥发 | ||
| C. | 蒸馏海水、氢气验纯 | D. | 金属冶炼、石灰石煅烧 |
6.下列装置使用不恰当的是( )
| A. |  实验室收集氢气 | B. |  用现有条件检查装置气密性 | ||
| C. |  证明CO2能与NaOH溶液反应 | D. |  探究燃烧的三个条件 |
13.下列各组物质按酸、碱、盐顺序排列的是( )
| A. | HNO3、Mg(OH)2、NaHCO3 | B. | NaOH、Na2CO3、HCl | ||
| C. | NaHCO3、Ca(OH)2、CuSO4 | D. | NaCl、Cu(OH)2、H2CO3 |
10.下列物质在水溶液中能大量共存的是( )
| A. | NH4Cl、Ca(OH)2、NaNO3 | B. | NaCl、K2CO3、H2SO4 | ||
| C. | HCl、BaCl2、FeSO4 | D. | K2SO4、NaOH、Na2CO3 |
11. 有一包白色固体,可能含有CaCO3、CuSO4、NaOH、BaCl2中的一种或几种.取样溶于水,有沉淀产生;过滤后向沉淀中滴加盐酸有气体产生,沉淀的量与加入盐酸体积的关系如图所示.由此推断白色固体中( )
有一包白色固体,可能含有CaCO3、CuSO4、NaOH、BaCl2中的一种或几种.取样溶于水,有沉淀产生;过滤后向沉淀中滴加盐酸有气体产生,沉淀的量与加入盐酸体积的关系如图所示.由此推断白色固体中( )
 有一包白色固体,可能含有CaCO3、CuSO4、NaOH、BaCl2中的一种或几种.取样溶于水,有沉淀产生;过滤后向沉淀中滴加盐酸有气体产生,沉淀的量与加入盐酸体积的关系如图所示.由此推断白色固体中( )
有一包白色固体,可能含有CaCO3、CuSO4、NaOH、BaCl2中的一种或几种.取样溶于水,有沉淀产生;过滤后向沉淀中滴加盐酸有气体产生,沉淀的量与加入盐酸体积的关系如图所示.由此推断白色固体中( )| A. | 沉淀一定有BaSO4和CaCO3,一定没有Cu(OH)2 | |
| B. | 沉淀如果有蓝色就说明白色固体中一定存在CuSO4,一定不存在BaCl2 | |
| C. | 白色固体肯定肯定存在CaCO3、BaCl2,可能存在CuSO4、NaOH | |
| D. | 白色固体中一定存在CaCO3、CuSO4、BaCl2,可能存在NaOH |
