题目内容
5.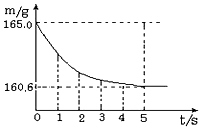 在烧杯中加入氯化钠和碳酸氢钠的固体混合物10.0g后,再加入73g稀盐酸恰好完全反应.反应过程用精密仪器测得烧杯连同药品的总质量(m)与反应时间(t)的关系如图所示.烧杯连同药品的起始总质量为165.0g.反应的方程式为NaHCO3+HCl=NaCl+H2O+CO2↑;试回答下列问题:
在烧杯中加入氯化钠和碳酸氢钠的固体混合物10.0g后,再加入73g稀盐酸恰好完全反应.反应过程用精密仪器测得烧杯连同药品的总质量(m)与反应时间(t)的关系如图所示.烧杯连同药品的起始总质量为165.0g.反应的方程式为NaHCO3+HCl=NaCl+H2O+CO2↑;试回答下列问题:(1)完全反应时产生二氧化碳的质量为4.4g.
(2)NaHCO3中碳元素的质量分数是14.3%
(3)稀盐酸中溶质的质量分数是多少?
(4)反应后所得氯化钠溶液中有氯化钠溶质7.45克.
分析 碳酸氢钠和稀盐酸反应生成氯化钠、水和二氧化碳,根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
解答 解:(1)完全反应时产生二氧化碳的质量为:165.0g-160.6g=4.4g.
故填:4.4.
(2)NaHCO3中碳元素的质量分数是:$\frac{12}{84}$×100%=14.3%,
故填:14.3%.
(3)设碳酸氢钠质量为x,氯化氢质量为y,生成氯化钠质量为z,
NaHCO3+HCl=NaCl+H2O+CO2↑,
84 36.5 58.5 44
x y z 4.4g
$\frac{84}{x}$=$\frac{36.5}{y}$=$\frac{58.5}{z}$=$\frac{44}{4.4g}$,
x=8.4g,y=3.65g,z=5.85g,
稀盐酸中溶质的质量分数是:$\frac{3.65g}{73g}$×100%=5%,
答:稀盐酸中溶质的质量分数是5%.
(4)反应后所得氯化钠溶液中氯化钠质量为:10.0g-8.4g+5.85g=7.45g,
故填:7.45.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
13.下列除杂(括号内为杂质)的实验过程正确的是( )
| A. | KCl(K2CO3) 加足量稀盐酸、过滤、蒸发、结晶 | |
| B. | MnO2(KC1)加水溶解、过滤、蒸发、结晶 | |
| C. | CuO(Cu) 加足量稀盐酸、过滤、洗涤、干燥 | |
| D. | BaSO4(BaCO3) 加足量稀盐酸、过滤、洗涤、干燥 |
20.关于有机物的叙述,下列说法正确的是( )
| A. | 有了有机物才有生命,构成生物体的物质全部都是有机物 | |
| B. | 有机物一定含有碳元素,含碳化合物一定属于有机物 | |
| C. | 家用液化气的主要成分是乙炔 | |
| D. | 自然界的一些无机物在一定条件下会合成简单的有机物 |
17.下列排列顺序正确的是( )
| A. |  | B. | 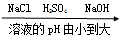 | ||
| C. |  | D. |  |
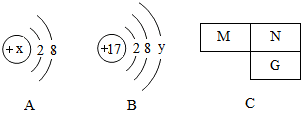
5.下列说法正确的是( )
| A. | 与酸反应产生二氧化碳气体的盐一定含有碳酸根 | |
| B. | 达稳定结构的原子最外层电子数一定为8 | |
| C. | 物质与氧气的反应一定属于氧化反应 | |
| D. | 碱中一定含有金属元素 |
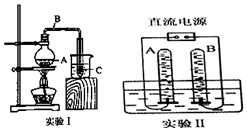
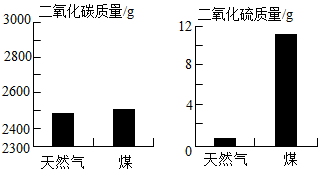 充分燃烧1kg天然气和煤所产生的CO2和SO2气体的质量如图所示,则煤燃烧产生的气体更易导致酸雨,天然气燃烧对环境影响较小.
充分燃烧1kg天然气和煤所产生的CO2和SO2气体的质量如图所示,则煤燃烧产生的气体更易导致酸雨,天然气燃烧对环境影响较小.