题目内容
10.根据下列装置回答问题.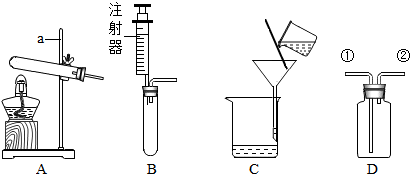
(1)仪器a的名称是铁架台.
(2)C是进行过滤操作装置中的一部分.
(3)若选用D装置收集CO2,则气体应从①(填“①”或“②”)端进入.利用该装置收集CO2时,为了检验CO2是否收集满的方法是将燃着的木条靠近②端(填“①”或“②”).若D装置中盛有澄清石灰水,则可以验证CO2气体,此反应的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O.
(4)若用高锰酸钾制取氧气,则应选择的发射装置是(填编号)A,且该发生装置中还缺少的实验用品是试管口放一团棉花,写出该反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(5)写出实验用B装置制二氧化碳的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
分析 (1)根据题中所指仪器的作用进行分析;
(2)根据题中进行的实验操作进行分析;
(3)根据二氧化碳密度比空气大,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水进行分析;
(4)根据实验室高锰酸钾制取氧气的反应物是固体,反应条件是加热,试管口需要放一团棉花,防止高锰酸钾粉末进入导管,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
(5)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,a是铁架台;
(2)通过分析题中的实验操作可知,C是进行过滤操作装置中的一部分;
(3)二氧化碳密度比空气大,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以选用D装置收集CO2,则气体应从①端进入.利用该装置收集CO2时,为了检验CO2是否收集满的方法是将燃着的木条靠近②端.若D装置中盛有澄清石灰水,则可以验证CO2气体,化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;
(4)实验室高锰酸钾制取氧气的反应物是固体,反应条件是加热,所以选择的反应装置是A,试管口需要放一团棉花,防止高锰酸钾粉末进入导管,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(5)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
故答案为:(1)铁架台;
(2)过滤;
(3)①,②,Ca(OH)2+CO2═CaCO3↓+H2O;
(4)A,试管口需要放一团棉花,2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(5)CaCO3+2HCl═CaCl2+H2O+CO2↑.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

 阅读快车系列答案
阅读快车系列答案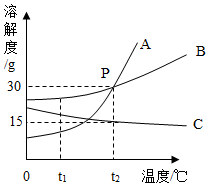 如图是A、B、C三种固体物质的溶解度曲线.下列说法正确的是( )
如图是A、B、C三种固体物质的溶解度曲线.下列说法正确的是( )| A. | 物质A的溶解度大于物质C的溶解度 | |
| B. | t2℃时.C物质的饱和溶液中溶质的质量分数为15% | |
| C. | 将t2℃时的A、B、C三种物质的饱和溶液降温到tl℃时所得溶液中溶质的质量分数的关系为;B>C>A | |
| D. | t2℃时.A、B两物质的溶液中溶质的质量分数相等 |

 已知A-G均为初中化学常见的物质.其中A、B的组成元素相同,D是形成温室效应的主要原因,F俗称纯碱,E和G只有阳离子不同.根据图中所示的转化关系(图中“-”表示相互间能反应,“→”表示在一定条件下能生成该物质,反应条件均已略去),请回答:
已知A-G均为初中化学常见的物质.其中A、B的组成元素相同,D是形成温室效应的主要原因,F俗称纯碱,E和G只有阳离子不同.根据图中所示的转化关系(图中“-”表示相互间能反应,“→”表示在一定条件下能生成该物质,反应条件均已略去),请回答: