题目内容
7.已知难溶性的碱受热易分解,生成金属氧化物和水(提示:分解过程中元素化合价不变化).X、Y、Z、E、W五种物质之间存在下图所示的转化关系:
请根据上图变化回答下列问题:
(1)X溶液中的溶质的成分为氯化铁(化学式).
(2)反应①化学方程式为3NaOH+FeCl3═Fe(OH)3↓+3NaCl.
(3)加稀HNO3的作用是除过量的氢氧化钠.
(4)反应③的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(5)上述4个反应中属于复分解反应的是①④(填序号).
分析 根据红褐色沉淀Y为氢氧化铁,而Z为氧化铁,Z与一氧化碳反应生成E铁,白色沉淀W为酸化后的溶液与硝酸银反应生成的沉淀,因此沉淀W为不溶于酸的沉淀,可推断为氯化银,结合反应框图可知,X溶液中含Cl-;而X与NaOH反应Fe(OH)3红褐色沉淀,所以X溶液中含有Fe3+;综上所述,物质X为氯化铁溶液;据此,可根据反应框图完成对其它物质的推断.
解答 解:
根据红褐色沉淀Y为氢氧化铁,而Z为氧化铁,Z与一氧化碳反应生成E铁,白色沉淀W为酸化后的溶液与硝酸银反应生成的沉淀,因此沉淀W为不溶于酸的沉淀,可推断为氯化银,结合反应框图可知,X溶液中含Cl-;而X与NaOH反应Fe(OH)3红褐色沉淀,所以X溶液中含有Fe3+;综上所述,物质X为氯化铁溶液;据此,可根据反应框图完成对其它物质的推断.
(1)根据分析,X溶液中的溶质的成分为氯化铁.
(2)反应①为氯化铁溶液与氢氧化钠反应生成氢氧化铁沉淀和氯化钠,反应的化学方程式为3NaOH+FeCl3═Fe(OH)3↓+3NaCl.
(3)加稀HNO3的作用是除过量的氢氧化钠.
(4)反应③为高温下CO还原氧化铁,生成铁和二氧化碳,故其化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(5)反应①为氯化铁溶液与氢氧化钠反应生成氢氧化铁沉淀和氯化钠,为复分解反应;
反应②为Fe(OH)3红褐色沉淀加热生成氧化铁和水,为分解反应;
反应③为高温下CO还原氧化铁,生成铁和二氧化碳,不是基本反应类型;
反应④为氯化钠与硝酸银反应生成氯化银沉淀和硝酸钠,为复分解反应.
故上述4个反应中属于复分解反应的是①④.
故答案为:
(1)氯化铁.(2)3NaOH+FeCl3═Fe(OH)3↓+3NaCl.
(3)除过量的氢氧化钠.(4)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.(5)①④
点评 根据特殊的现象或特殊的反应或特殊的物质颜色,找到推断类题的解决突破口,是解决此类问题的主要手段.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 16g | B. | 22g | C. | 44g | D. | 88g |
【猜想与假设】
①氢氧化钠没有变质;②该氢氧化钠部分变质;③该氢氧化钠全部变质.
【设计实验】取氢氧化钠固体样品溶于水配成溶液A,进行如下实验:
| 实验步骤 | 实验现象 | 结论及解释 |
| (1)取少量溶液A于试管中,向其中滴加足量的稀盐酸 | 有气泡产生 | 猜想①不成立 |
| (2)另取少量溶液A于试管中,向其中滴加足量的氯化钙溶液 | 产生白色沉淀 | 反应的化学方程式为Na2CO3+CaCl2=CaCO3↓+2NaCl |
| (3)将步骤(2)所得的混合液静置,向上层清液中滴加无色的酚酞溶液 | 溶液呈红色 | 猜想②成立 |
(4)久置的氢氧化钠变质的原因是(用化学方程式表示)CO2+2NaOH=Na2CO3+H2O.
【探索与拓展】(5)为进一步探究氢氧化钠的变质程度,小明称取18.6g氢氧化钠固体样品放入烧杯中,向其中逐滴加入稀盐酸,到不再产生气泡为止,共消耗稀盐酸100g,反应后称得烧杯中溶液的质量为115.6g.求该样品中碳酸的质量分数(要写出计算过程).
 某兴趣小组为验证质量守恒定律,除了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,除了镁条在空气中燃烧的实验.(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)镁条完全燃烧后,小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律,我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①通过查阅资料,记录了下列几种物质的颜色:
| 物质 | MgO | MgCl2 | Mg3N2 |
| 颜色 | 白色 | 白色 | 淡黄色 |
【做出猜想】黄色固体是Mg3N2
【实验探究】请你设计实验方案,验证猜想:将镁条放在纯净的氮中点燃,产生黄色固体,证明产物是氮化镁.
【反思与交流】①小华同学认为,在查阅资料时,有一种物质完全可以不用考虑,请推断该物质是氯化镁(填名称),你的理由是空气中不含氯元素;
②写出镁条与氮气反应的化学方程式3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;
③空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成MgO却远多于Mg3N2,为什么呢?请给出合理的解释氧气的化学性质比氮气更活泼.
资料:硝酸钾的溶解度数据(部分数据已做取整数处理)如表所示:
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 溶解度/g | 21 | 32 | 46 | 64 | 86 | 110 | 138 |
(2)A、B、C、D四个烧杯中分别盛有100g水,在40℃时,向四个烧杯中分别加入110g、86g、64g、32g硝酸钾,充分溶解,如图所示.

①(填字母序号)ABC中盛的一定是饱和溶液.
②使B烧杯的溶液升温至50℃时,溶液的质量为186 g.
③采用一种方法使A中的固体恰好溶解.对于最终四个烧杯中的溶液,下列说法正确的是acd(填字母序号).
a.溶剂质量可能相等
b.溶质质量可能相等
c.溶质质量分数可能有相等的
d.烧杯A中的溶液质量分数可能最大
(3)工业上利用电解饱和氯化钠溶液可制得重要化工产品氢氧化钠.氢氧化钠溶液可用于治理含二氧化硫的废气并回收二氧化硫,反应的主要流程如下:

①实际生产中,在一定温度下,配制100t溶质的质量分数为25%的饱和氯化钠溶液,需水的质量为75t.
②以上流程中,可循环使用的物质是氯化钠(NaCl).
③亚硫酸氢钠(NaHSO3)中硫元素的质量分数为30.8%(计算结果精确到0.1%).
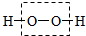 ②H-O-H ③O=C=O ④
②H-O-H ③O=C=O ④