题目内容
4.现有一包固体粉末,可能是NaOH、Na2CO3、Na2SO4、CuSO4、NaCl中的一种或几种,为确定其组成,取适量试样进行下列实验.请根据实验现象判断:(1)取试样溶于水,得到无色澄清溶液,由此得出固体粉末中一定没有硫酸铜;
(2)取上述溶液适量,滴加过量的Ba(NO3)2溶液,出现白色沉淀,经过滤得固体A和滤液B;再向A中加入过量的稀硝酸,沉淀部分消失并产生气泡.经过滤得滤液C.则此固体粉末中一定有:硫酸钠、碳酸钠,形成沉淀的一个方程式:Na2CO3+Ba(NO3)2=BaCO3↓+2NaNO3或 Na2SO4+Ba(NO3)2=BaSO4↓+2NaNO3;
(3)取步骤(2)实验后的滤液C,加入稀硝酸、硝酸银溶液,无现象,由此该同学得出此固体粉末中不含NaCl,你认为此结论是否正确是(填“是”或“否”);
(4)对于是否含有NaOH,取滤液B于试管中,接下操作是:加入酚酞试液,出现溶液变红 则含氢氧化钠.
分析 (1)根据硫酸铜溶液呈蓝色分析
(2)根据碳酸钠与硝酸钡反应生成碳酸钡沉淀,硫酸钠与硝酸钡反应生成硫酸钡沉淀,碳酸钡溶于酸,而硫酸钡不溶于酸进行分析;
(3)根据氯离子与银离子结合生成不溶于稀硝酸的氯化银沉淀分析
(4)根据氢氧化钠溶液呈碱性分析.
解答 解:(1)试样溶于水,得到无色澄清溶液,因为硫酸铜溶于水溶液呈蓝色,所以固体粉末中一定没有硫酸铜;
(2)取溶液适量,滴加过量的Ba(NO3)2溶液,出现白色沉淀,硝酸钡与碳酸钠反应生成碳酸钡沉淀,硝酸钡与硫酸钠反应生成硫酸钡沉淀,碳酸钠与稀硝酸反应产生二氧化碳气体,硫酸钡与稀硝酸不反应,向沉淀A中加入过量的稀硝酸,沉淀部分消失并产生气泡.则固体中一定含有碳酸钠和硫酸钠;形成沉淀的化学方程式为:
Na2CO3+Ba(NO3)2=BaCO3↓+2NaNO3; Na2SO4+Ba(NO3)2=BaSO4↓+2NaNO3
(3)取步骤(2)实验后的滤液C,加入稀硝酸、硝酸银溶液,无现象,说明溶液C中不含氯离子,由于整个实验过程中没有另外加入氯离子,所以可以得出固体粉末中不含NaCl,此结论是正确的.
(4)滤液B中一定含有硝酸钠,若加入酚酞试液,溶液变红,则固体中一定含有氢氧化钠.
故答案为:(1)硫酸铜(2)硫酸钠、碳酸钠Na2CO3+Ba(NO3)2=BaCO3↓+2NaNO3或Na2SO4+Ba(NO3)2=BaSO4↓+2NaNO3
(3)是;
(4)酚酞试液,溶液变红 氢氧化钠
点评 在解此类题时,首先根据题中的现象确定一定存在或一定不存在的物质,对于检验离子是不能引入后面还要检验的离子

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
14.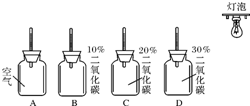 某校科技小组为探究不同浓度CO2的温室效应,设计了下图所示的实验装置.A瓶内充满普通空气,B、C、D三瓶内分别充有含10%、20%、30% CO2的空气,放在黑暗处一昼夜,实验时在一排集气瓶的右侧上方用功率为200W的灯泡照射,10分钟后观察温度计的读数.然后再将四个集气瓶避光保存10分钟,再次观察温度计的读数.试回答:
某校科技小组为探究不同浓度CO2的温室效应,设计了下图所示的实验装置.A瓶内充满普通空气,B、C、D三瓶内分别充有含10%、20%、30% CO2的空气,放在黑暗处一昼夜,实验时在一排集气瓶的右侧上方用功率为200W的灯泡照射,10分钟后观察温度计的读数.然后再将四个集气瓶避光保存10分钟,再次观察温度计的读数.试回答:
(1)小明同学认为实验中有一处明显需要改进,存在的问题是灯泡放在一排集气瓶的右侧上方.
(2)实验改进后,测得的数据如下:
结合表中实验数据,该实验可以得到的结论是在同一时间内CO2含量越高,温度升高的越高.
(3)反思与评价:要控制温室效应加剧,可以采取的措施有随手关灯(试列出一条).
 某校科技小组为探究不同浓度CO2的温室效应,设计了下图所示的实验装置.A瓶内充满普通空气,B、C、D三瓶内分别充有含10%、20%、30% CO2的空气,放在黑暗处一昼夜,实验时在一排集气瓶的右侧上方用功率为200W的灯泡照射,10分钟后观察温度计的读数.然后再将四个集气瓶避光保存10分钟,再次观察温度计的读数.试回答:
某校科技小组为探究不同浓度CO2的温室效应,设计了下图所示的实验装置.A瓶内充满普通空气,B、C、D三瓶内分别充有含10%、20%、30% CO2的空气,放在黑暗处一昼夜,实验时在一排集气瓶的右侧上方用功率为200W的灯泡照射,10分钟后观察温度计的读数.然后再将四个集气瓶避光保存10分钟,再次观察温度计的读数.试回答:(1)小明同学认为实验中有一处明显需要改进,存在的问题是灯泡放在一排集气瓶的右侧上方.
(2)实验改进后,测得的数据如下:
| 温度计标号 | A | B | C | D |
| 初始温度 | 18℃ | 18℃ | 18℃ | 18℃ |
| 10分钟后温度 | 20 | 21℃ | 22℃ | 23℃ |
| 避光保存10分钟后的温度 | 18.5℃ | 19.5℃ | 21℃ | 22.5℃ |
(3)反思与评价:要控制温室效应加剧,可以采取的措施有随手关灯(试列出一条).
15.某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②沼气和水蒸气都是可再生能源;③使用车用乙醇汽油防止“温室效应;④不锈钢和目前流通的硬币都是合金;⑤推广使用无氟冰箱防止“臭氧空洞”;⑥纯碱和熟石灰都是碱;⑦生成盐和水的反应一定是中和反应.其中说法完全正确的组合是( )
| A. | ①③④⑤ | B. | ①②⑤⑥ | C. | ③⑤⑥⑦ | D. | ①④⑤ |
12. 实验室有半瓶敞口放置的标签残缺的白色固体(标签如图),小明、小亮根据初中所学的知识进行下列探究.
实验室有半瓶敞口放置的标签残缺的白色固体(标签如图),小明、小亮根据初中所学的知识进行下列探究.
【交流讨论Ⅰ】(1)小明与小亮一致认为碱石灰的用途能做干燥剂,理由是碱石灰中的生石灰和火碱都有吸水性.
(2)取适量该固体放入烧杯中,加入适量的水充分搅拌,发现烧杯中有白色沉淀,烧杯外壁发热,于是小亮得出结论一定有生石灰.小明认为不一定,小明的理由是火碱溶于水也会放热..
(3)他俩将(2)烧杯中的混合物过滤,对滤液和白色沉淀的组成情况进行了进一步探究.
【猜测】
(1)小明猜测滤液中的溶质是:
①NaOH ②Ca(OH)2 ③NaOH、Ca(OH)2 ④Ca(OH)2、Na2CO3 ④Na2CO3、NaOH
【交流讨论Ⅱ】小亮认为小明的猜测中②④不合理(填序号),小亮猜测滤液中的溶质还可能是Na2CO3.
【活动探究】小明刘滤液中的溶质的成分进行探究(资料:BaCl2溶液显中性,BaC03为不溶于水的白色固体)
(2)小亮猜测白色沉淀是:
①CaCO3 ②CaCO3、Ca(OH)2
【交流讨论Ⅲ】小亮根据小明的实验结论得出自己对白色沉淀的猜测中①正确(填序号).
【启示】药品保存时应注意应密闭保存.
 实验室有半瓶敞口放置的标签残缺的白色固体(标签如图),小明、小亮根据初中所学的知识进行下列探究.
实验室有半瓶敞口放置的标签残缺的白色固体(标签如图),小明、小亮根据初中所学的知识进行下列探究.【交流讨论Ⅰ】(1)小明与小亮一致认为碱石灰的用途能做干燥剂,理由是碱石灰中的生石灰和火碱都有吸水性.
(2)取适量该固体放入烧杯中,加入适量的水充分搅拌,发现烧杯中有白色沉淀,烧杯外壁发热,于是小亮得出结论一定有生石灰.小明认为不一定,小明的理由是火碱溶于水也会放热..
(3)他俩将(2)烧杯中的混合物过滤,对滤液和白色沉淀的组成情况进行了进一步探究.
【猜测】
(1)小明猜测滤液中的溶质是:
①NaOH ②Ca(OH)2 ③NaOH、Ca(OH)2 ④Ca(OH)2、Na2CO3 ④Na2CO3、NaOH
【交流讨论Ⅱ】小亮认为小明的猜测中②④不合理(填序号),小亮猜测滤液中的溶质还可能是Na2CO3.
【活动探究】小明刘滤液中的溶质的成分进行探究(资料:BaCl2溶液显中性,BaC03为不溶于水的白色固体)
| 实验步骤 | 实验现象 | 结论 |
| A.取少量滤液加入过量的BaCl2溶液 | 产生白色沉淀 | 一定有Na2CO3 |
| B.将A中的混合物过滤,向滤液中加酚酞试液 | 溶液变成红色 | 一定有NaOH |
①CaCO3 ②CaCO3、Ca(OH)2
【交流讨论Ⅲ】小亮根据小明的实验结论得出自己对白色沉淀的猜测中①正确(填序号).
【启示】药品保存时应注意应密闭保存.
19.分类是学习化学的方法之一,下列物质是按单质、碱、混合物的顺序排列的是( )
| A. | 氧气、纯碱、空气 | B. | 氢气、硫酸、石灰水 | ||
| C. | 水、烧碱、生铁 | D. | 铜丝、熟石灰、石油 |
13.焊接金属时,能做保护气的一组是( )
| A. | H2、N2 | B. | N2、O2 | C. | CO、CO2 | D. | N2、Ar(氩气) |
14.几种作物适宜生长的pH范围如表.取某地土壤浸出液,用pH试纸测得其显碱性.则这种土壤适宜种植的作物是( )
| 作物 | 茶树 | 棉花 | 水稻 | 甘草 |
| pH | 5.0~5.5 | 6.0~6.8 | 6.0~7.0 | 7.2~8.5 |
| A. | 水稻 | B. | 棉花 | C. | 茶树 | D. | 甘草 |