题目内容
20.某学校研究性学习小组,以一工厂生产过程中产生的废弃物“红色铁泥”为研究对象,探究红色物质的成分,请你参与他们的活动.[小组讨论]
甲观点:红色物质是铜. 乙观点:红色物质是氧化铁.
丙观点:红色物质是氢氧化铁. 丁观点:红色物质是氧化铁和氢氧化铁的混合物.
[查阅资料]
该厂“红色铁泥”主要是生产过程中使用铁触媒(一种催化剂)后的废弃物,除红色物质外,还含有通常不与酸、碱和氧气反应的物质.氢氧化铁受热易分解
[提出假设]?
乙、丙、丁三种观点存在合理性.
[实验验证]
Ⅰ取适量“红色铁泥”晒干,称量其质量为m1克;
Ⅱ将“红色铁泥”置于坩埚中充分加热并在干燥器中冷却后,称量其质量为m2克.
请回答下列问题:
(1)当m1=m2时,则红色物质为氧化铁.
(2)当m1>m2>$\frac{160{m}_{1}}{214}$时,则“红色铁泥”中一定含有氧化铁吗?不一定(填写“一定”或“不一定”),理由是“红色铁泥”有可能含有其他不溶性或受热不分解的杂质.
(3)假定“红色铁泥”中“红色物质是氢氧化铁”,请写出回收“红色铁泥”中的铁元素制得“铁红”(化学式为Fe2O3,是红色油漆的重要原料)过程中的化学反应最少需要3(填数字)次.
分析 根据题干提供的信息,该废弃物除杂质外可能还含有铜、氧化铁、氢氧化铁或氧化铁和氢氧化铁的混合物,
Fe(OH)3、Fe2O3,Fe(OH)3难溶于水,受热发生分解反应而导致固体质量减少,加热后固体质量是否增加是确定是否含有氢氧化铁的标志,铜加热生成氧化铜,固体质量增加,加热后固体质量是否增加定固体是否为铜,氧化铁加热质量没有变化.
解答 解:(1)由于红色物质加热质量不变,故该物质不可能是铜或氢氧化铁,只能是氧化铁,所以当m1=m2时,红色物质为氧化铁;
(2)氢氧化铁加热后生成氧化铁和水,固体质量减少,当m1>m2时,“红色铁泥”中一定含有氢氧化铁,
假设全部为氢氧化铁,
2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O
214 160
m1 m2 m2=160m1/214
因为m1>m2>160m1/214,所以“红色铁泥”中不全是氢氧化铁,但不一定有氧化铁,有可能含有其他不溶性或受热不分解的杂质;
(3)回收“红色铁泥”中的铁元素制得“铁红”需要将氢氧化铁与盐酸反应生成氯化铁和水,之后氯化铁与氢氧化钠反应生成氢氧化铁沉淀和氯化钠,最后氢氧化钠加热生成氧化铁和水,化学方程式为:①Fe(OH)3+3HCl=FeCl3+3H2O,②FeCl3+3NaOH=Fe(OH)3↓+3NaCl,③2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O.
故答案为:(1)氧化铁(Fe2O3).
(2)不一定,“红色铁泥”有可能含有其他不溶性或受热不分解的杂质.
(3)3
点评 本题是一种开放性试题,解题时一定要找准角度,完成此题,可以依据已有的知识进行.

 同步练习强化拓展系列答案
同步练习强化拓展系列答案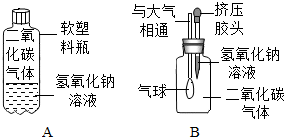 某化学课堂上同学们正在进行酸、碱、盐知识的探究,以下是教学片断,请你参与其中并认真填写空格.
某化学课堂上同学们正在进行酸、碱、盐知识的探究,以下是教学片断,请你参与其中并认真填写空格.【学生实验】将二氧化碳分别通入澄清石灰水和氢氧化钠溶液中,观察到前者变浑浊,后者无明显现象.
【学生板演】澄清石灰水变浑浊的原理CO2+Ca(OH)2═CaCO3↓+H2O (用化学方程式表示).
【提出问题】二氧化碳通入氢氧化钠溶液中无明显现象,两者是否发生了化学反应?
【猜想假设】猜想①:两者发生了化学反应;猜想②:两者没有发生化学反应
【实验探究】(1)小华设计了如图所示的A、B两个实验.
实验现象:A中软塑料瓶変瘪,B中气球膨胀变大.
(2)小红认为小华的实验是可行的,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低.小明同学却对此提出质疑,他认为小华的实验不严谨,其理由是二氧化碳能与水反应或溶于水,也能使容器内压强降低,要得到科学严谨的结论,仍利用该装置,补做的对比实验是将氢氧化钠溶液换成等体积的水,与加入氢氧化钠溶液的实验现象进行对比.
(3)小宁设计的是通过检验生成物来验证猜想,请帮她填写实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| 向B实验后的溶液中加入稀盐酸(或氯化钙溶液等) | 有气泡产生(或有白色沉淀生成等) | 验证了二氧化碳和氢氧化钠溶液反应 |
【反思拓展】通过此探究实验,我们发现,对于没有明显现象的化学反应,可以从两个不同的角度证明反应的发生,这两个角度是可以通过检验反应物减少证明反应发生,可以通过检验生成物证明反应发生.
| A. | 红纸剪成窗花 | B. | 棉线织成衣服 | C. | 钢丝制成鱼钩 | D. | 玉米酿成白酒 |
| A. | 人体缺铁可能引起贫血 | |
| B. | 瘦肉和蛋清中都富含蛋白质 | |
| C. | 食用甲醛浸泡过的海产品,会危害人体健康 | |
| D. | 油脂是人体重要的供能物质,摄入越多越好 |
 如图是某试剂瓶标签的部分内容.请回答下列问题:
如图是某试剂瓶标签的部分内容.请回答下列问题: 我市某品牌矿泉水,其外包装上部分文字说明如图所示.请回答下列问题:
我市某品牌矿泉水,其外包装上部分文字说明如图所示.请回答下列问题: