题目内容
各种物质之间存在着某种联系.用A代替“>”,B代替“<”,C代替“=”,请分别选用“A”、“B”或“C”填在下列横线上.
(1)煮沸的浓硫酸的温度______煮沸的水的温度
(2)硫离子的核外电子数______氟离子的核外电子数.
(3)醋酸(C2H4O2)的含碳量______葡萄糖(C6H12O6)的含碳量
(4)铁元素的质量分数:氧化铁______氧化亚铁.
解:
(1)浓硫酸溶于水释放出大量的热,故煮沸的浓硫酸的温度大于煮沸的水的温度;
(2)硫原子核外有16个电子,最外层得到2个电子后变成硫离子,硫离子核外有18个电子;氟原子核外9个电子,得1个电子形成氟离子,氟离子核外有10个电子;故硫离子的核外电子数大于氟离子的核外电子数;
(3)醋酸(C2H4O2)中C元素的质量分数=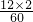 ×100%=40%;葡萄糖(C6H12O6)中C元素的质量分数=
×100%=40%;葡萄糖(C6H12O6)中C元素的质量分数= ×100%=40%;故两物质中含碳量相等;
×100%=40%;故两物质中含碳量相等;
(4)氧化亚铁中铁元素的质量分数为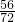 ×100%,氧化铁中铁元素的质量分数为
×100%,氧化铁中铁元素的质量分数为 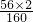 ×100%=
×100%=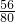 ×100%<
×100%<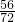 ×100%.
×100%.
故答案为:(1)A;(2)A;(3)C;(4)B.
分析:(1)浓硫酸溶于水释放出大量的热,据此分析判断;
(2)非金属元素硫的原子最外层得到2个电子后变成带2个单位负电荷的硫离子,而非金属元素氟的原子得到1个电子后形成带1个单位负电荷的氟离子;
(3)根据两物质的化学式,由组成元素的质量分数计算公式,计算出两物质中碳元素的质量分数;
(4)根据化合物中元素的质量分数的计算公式可以计算出铁元素的质量分数,进行比较分析.
点评:本题难度不大,考查知识比较全面,掌握核外电子排布、元素的质量分数等知识是正确解答本题的关键.
(1)浓硫酸溶于水释放出大量的热,故煮沸的浓硫酸的温度大于煮沸的水的温度;
(2)硫原子核外有16个电子,最外层得到2个电子后变成硫离子,硫离子核外有18个电子;氟原子核外9个电子,得1个电子形成氟离子,氟离子核外有10个电子;故硫离子的核外电子数大于氟离子的核外电子数;
(3)醋酸(C2H4O2)中C元素的质量分数=
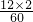 ×100%=40%;葡萄糖(C6H12O6)中C元素的质量分数=
×100%=40%;葡萄糖(C6H12O6)中C元素的质量分数= ×100%=40%;故两物质中含碳量相等;
×100%=40%;故两物质中含碳量相等;(4)氧化亚铁中铁元素的质量分数为
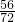 ×100%,氧化铁中铁元素的质量分数为
×100%,氧化铁中铁元素的质量分数为 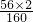 ×100%=
×100%=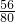 ×100%<
×100%<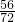 ×100%.
×100%.故答案为:(1)A;(2)A;(3)C;(4)B.
分析:(1)浓硫酸溶于水释放出大量的热,据此分析判断;
(2)非金属元素硫的原子最外层得到2个电子后变成带2个单位负电荷的硫离子,而非金属元素氟的原子得到1个电子后形成带1个单位负电荷的氟离子;
(3)根据两物质的化学式,由组成元素的质量分数计算公式,计算出两物质中碳元素的质量分数;
(4)根据化合物中元素的质量分数的计算公式可以计算出铁元素的质量分数,进行比较分析.
点评:本题难度不大,考查知识比较全面,掌握核外电子排布、元素的质量分数等知识是正确解答本题的关键.

练习册系列答案
相关题目
根据如图装置图,回答有关问题:

(1)写出装置图中标号仪器的名称:①______;②______.
(2)写出实验室用大理石和稀盐酸制取二氧化碳的化学方程式______.并据此选择上图中______(填字母)组装一套制取干燥二氧化碳的装置.
(3)小宇同学发现氯化铁溶液加入过氧化氢溶液中有大量气泡产生,于是就想氯化铁溶液也能用作催化剂,氯化铁溶液中有
Fe3+,Cl-,H2O三种微粒,是哪个微粒有催化作用呢?大家讨论后认为H2O没有催化作用,理由是______.
| 实验步骤 | 实验现象 | 试验结论 |
| 向过氧化氢溶液中加入氯化钠溶液 | 无明显现象 | Cl-没有催化作用 |
| 向过氧化氢溶液中加入氯化铁溶液 | 有大量的气泡产生 | ______ |
铁、铝、铜是日常生活中使用很广泛的三种金属.
(1)上述金属中,人类最早大规模冶炼和使用的是铜,最晚的是铝,原因是______(填序号).
A.三者在地壳中的含量,铜元素最高,铝元素最低
B.三者的金属活动性,铜元素最弱,铝元素最强
C.在自然界中,铜元素主要以单质形式存在,铝元素以化合物形式存在
(2)常温下一些金属的物理性质数据如下:
| 金属单质 | 铜 | 铝 | 锌 | 铁 | 铅 |
| 导电性(以银的导电性为100作标准) | 99 | 61 | 27 | 17 | 7.9 |
| 密度/(g?cm-3) | 8.92 | 2.70 | 7.14 | 7.86 | 11.3 |
| 熔点/℃ | 1083 | 660 | 419 | 1535 | 328 |
| 硬度(以金刚石的硬度为10作标准) | 2.5-3 | 2-2.9 | 2.5 | 4-5 | 1.5 |
(3)铜器长期暴露在空气中,表面会生成铜绿______,从其组成分析,预测铜变成铜绿是因为铜与空气中的______(任举一例)反应.
(4)工业上炼铜的一个主要反应是Cu2S+O2
 2Cu+SO2.Cu2S中铜元素的质量分数为______.用500吨含Cu2S 80%的铜矿石,理论上可以炼出______吨铜.
2Cu+SO2.Cu2S中铜元素的质量分数为______.用500吨含Cu2S 80%的铜矿石,理论上可以炼出______吨铜. 