题目内容
17.图1是元素周期表的一部分,据此回答下列问题.
(1)图1中13号元素的名称是铝,该元素的原子在化学反应中易失去(填“得到”或“失去”)电子,形成离子,其离子符号是Al3+.
(2)图2是元素锶(Sr)的原子结构示意图,则x=38,锶元素的氯化物的化学式为SrCl2.通过上表分析可知,锶元素位于元素周期表第5周期.
(3)表中不同种元素最本质的区别是a(填序号):
a:质子数不同 b:中子数不同 c:相对原子质量不同 d:电子数不同.
分析 (1)根据原子序数=核电荷数=质子数,由元素周期表中原子结构示意图的核内质子数进行分析解答;若最外层电子数≥4,则一般为非金属元素,在化学反应中易得电子,若最外层电子数<4,则一般为金属元素,在化学反应中易失去电子;
(2)当质子数=核外电子数,为原子;化合物化学式的书写一般规律:金属在前,非金属在后;氧化物中氧在后,原子个数不能漏,正负化合价代数和为零.通过上表分析可知,同一周期元素的原子核外电子层数与周期数相同,据此进行分析解答;
(3)根据不同种元素最本质的区别是质子数不同,进行解答.
解答 解:(1)根据原子序数=核电荷数=质子数,表中13号元素的原子结构示意图中,核内质子数为13,其元素的名称为铝元素;该元素的原子最外层电子数为3,在化学反应中易失去3个电子,形成阳离子,离子符号为Al3+;故填:铝;失去;Al3+;
(2)当质子数=核外电子数,为原子,由锶(Sr)的原子结构示意图,则x=2+8+18+8+2=38.锶元素的最外层电子数为2,在发生化学反应时易失去2个电子形成带2个单位正电荷的离子,其化合价为为+2价,氯元素显-1价,其氯化物的化学式为:SrCl2.通过上表分析可知,同一周期元素的原子核外电子层数与周期数相同,锶元素的原子核外有5个电子层,位于元素周期表的第5周期.
故填:38;SrCl2;5;
(3)根据不同种元素最本质的区别是质子数不同,故填:a.
点评 本题考查学生对元素周期表、原子结构示意图及其意义的理解,明确元素周期表的含义、原子中核内质子数和核外电子数之间的关系是解题的关键.

练习册系列答案
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
12.下列各种物质中,由离子构成的是( )
| A. | Fe | B. | H2O | C. | CO2 | D. | NaCl |
12.在实验室里制取氧气,即可采用分解过氧化氢的方法,也可采用分解氯酸钾的方法.上述两种方法的主要共同点有( )
(1)采用二氧化锰均可改变其反应速率;(2)反应都不需加热;
(3)都利用含氧化合物分解来达到目的;(4)两种方法所需仪器相同.
(1)采用二氧化锰均可改变其反应速率;(2)反应都不需加热;
(3)都利用含氧化合物分解来达到目的;(4)两种方法所需仪器相同.
| A. | (2)(4) | B. | (3)(4) | C. | (1)(2) | D. | (1)(3) |
2.下列实验操作正确的是( )
| A. | 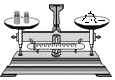 称量固体 | B. | 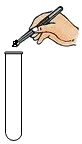 取用块状固体 | C. |  过滤 | D. |  检查装置气密性 |
9. 如图是电解水的装置,下列关于电解水实验的说法正确的是( )
如图是电解水的装置,下列关于电解水实验的说法正确的是( )
 如图是电解水的装置,下列关于电解水实验的说法正确的是( )
如图是电解水的装置,下列关于电解水实验的说法正确的是( )| A. | 水中加入少量的硫酸或氢氧化钠可以增强导电性 | |
| B. | 1是电源的负极 | |
| C. | 用燃着的木条检验产生的气体,a气体能燃烧,b气体能使木条燃烧的更旺 | |
| D. | 实验得出水由氢原子和氧原子构成的 |
6.下列各组日常生活中发生的变化,全部属于化学变化的一组是( )
| A. | 煤气燃烧 水变蒸气 | B. | 菜刀生锈 水果腐烂 | ||
| C. | 瓷碗破碎 剩饭变馊 | D. | 灯泡发光 冰块熔化 |

 硫酸亚铁(FeSO4)是常见补铁类保健品中的有效成分之一.
硫酸亚铁(FeSO4)是常见补铁类保健品中的有效成分之一. A-G是初中常见的几种物质,它们有如图所示的转化关系,已知A、C是无色液体且含有的元素种类相同,B、F是无色气体,其中F能使澄清石灰水变浑浊,E在纯净的B中燃烧火星四射,回答下列问题:
A-G是初中常见的几种物质,它们有如图所示的转化关系,已知A、C是无色液体且含有的元素种类相同,B、F是无色气体,其中F能使澄清石灰水变浑浊,E在纯净的B中燃烧火星四射,回答下列问题: