题目内容
5.某化学兴趣小组为测定某大理石样品中碳酸钙的含量,将适量的稀盐酸加入20g大理石中(其它成分不与盐酸反应),再将产生的CO2气体用足量的澄清石灰水吸收,同时测量2分钟内石灰水增加的质量,结果如下表所示:| 时间/s | 0 | 20 | 40 | 60 | 80 | 100 | 120 |
| 石灰水增加的质量/g | 0 | 3.0 | 5.0 | 6.0 | 6.6 | 6.6 | 6.6 |
(2)CO2刚好被澄清石灰水完全吸收的时间是80秒
(3)计算大理石样品中碳酸钙的质量分数.(写出计算过程)
分析 由图表数据可知,石灰水增加的质量到80s时不再变化,说明CO2气体已被澄清石灰水吸收完;由质量守恒定律可知,石灰水增加的质量就是产生二氧化碳气体的质量;
根据碳酸钙与盐酸反应的化学方程式和生成的二氧化碳的质量,列出比例式,就可计算出样品中碳酸钙的质量;然后根据质量分数公式计算即可.
解答 解:(1)由图表数据可知,共产生二氧化碳气体的质量为6.6g;
(2)由图表数据可知,石灰水增加的质量到80s时不再变化,说明CO2刚好被澄清石灰水完全吸收的时间是80s,故填:80;
(3)解:设样品中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 6.6g
$\frac{100}{44}=\frac{x}{6.6g}$
解之得:x=15g;
样品中碳酸钙的质量分数=$\frac{15g}{20g}$×100%=75%.
答:大理石样品中碳酸钙的质量分数为75%.
点评 本题主要考查学生利用化学方程式和质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
4.下列物质能与硫酸溶液发生复分解反应,而且效果明显的是( )
| A. | 无锈铁钉 | B. | 完全锈蚀的铁钉 | C. | 铜钉 | D. | 硫酸铜 |
20. CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?某化学兴趣小组的同学们对此进行了探究.
CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?某化学兴趣小组的同学们对此进行了探究.
【查阅资料】
①通常情况下,1体积水溶解1体积的CO2. ②在一定浓度的溶液中,有微溶物生成的复分解反应也能发生.
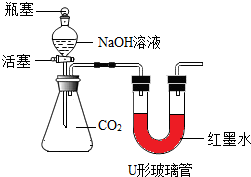
【实验探究】小红同学设计了如图所示的实验装置(锥形瓶内充满CO2),并进行实验.
打开瓶塞和活塞,使NaOH溶液快速滴入锥形瓶中,立即关闭活塞(漏斗中仍有溶液剩余),观察到U形管左侧的红墨水液面升高(填“升高”、“降低”或“不移动”),小红根据现象判断CO2和NaOH发生了反应,写出CO2与NaOH溶液反应的化学方程式:2NaOH+CO2=Na2CO3+H2O;
【反思与评价1】小明认为小红的实验方案不严密,理由是二氧化碳溶于水(或与水发生反应)也会使锥形瓶内气压减小;
【拓展实验】兴趣小组的同学们为此又设计了下表所示的两种方法,进一步探究.请填写表中的空格.
【反思与评价2】同学们经过讨论,认为拓展实验的方法一(填“方法一”或“方法二”)依然不严密,理由是CaCl2+2NaOH=Ca(OH)2↓+2NaCl.
 CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?某化学兴趣小组的同学们对此进行了探究.
CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?某化学兴趣小组的同学们对此进行了探究.【查阅资料】
①通常情况下,1体积水溶解1体积的CO2. ②在一定浓度的溶液中,有微溶物生成的复分解反应也能发生.
【实验探究】小红同学设计了如图所示的实验装置(锥形瓶内充满CO2),并进行实验.
打开瓶塞和活塞,使NaOH溶液快速滴入锥形瓶中,立即关闭活塞(漏斗中仍有溶液剩余),观察到U形管左侧的红墨水液面升高(填“升高”、“降低”或“不移动”),小红根据现象判断CO2和NaOH发生了反应,写出CO2与NaOH溶液反应的化学方程式:2NaOH+CO2=Na2CO3+H2O;
【反思与评价1】小明认为小红的实验方案不严密,理由是二氧化碳溶于水(或与水发生反应)也会使锥形瓶内气压减小;
【拓展实验】兴趣小组的同学们为此又设计了下表所示的两种方法,进一步探究.请填写表中的空格.
| 实验方法 | 操作过程 | 现象 | 实验结论 |
| 方法一 | 取小红实验后锥形瓶内的溶液适量,加入足量CaCl2溶液 | 有白色沉淀生成 | CO2与NaOH发生了反应 |
| 方法二 | 取小红实验后锥形瓶内的溶液适量,加入足量稀硫酸 | 有气泡冒出 |
17.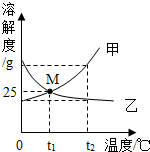 如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法错误的( )
如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法错误的( )
 如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法错误的( )
如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法错误的( )| A. | 乙的饱和溶液由t2℃降温到t1℃时,溶质的质量分数不变 | |
| B. | 甲中含有少量乙,可以用冷却热饱和溶液的方法提纯甲 | |
| C. | t1℃时,50g水中分别加入25g的甲、乙,均可得到75g的饱和溶液 | |
| D. | t1℃时,等质量甲、乙两物质的饱和溶液蒸发等质量的水,所得溶液中溶质的质量一定相等 |
8.有X、Y、Z、W四种金属,已知用X制的容器不能盛放Z的金属化合物溶液;X跟Y的化合物溶液不发生置换反应;只有W在自然界中能以单质的形式存在.则这四种金属的活动性顺序是( )
| A. | Z>Y>X>W | B. | X>Z>Y>W | C. | Y>X>Z>W | D. | Y>Z>X>W |