题目内容
14.工业过氧化氢溶液中过H2O2的质量分数通常为20~80%.某厂化验室为了测定某批过氧化氢溶液中H2O2的质量分数,进行了以下分析实验:称取溶液样品注入烧杯中,将称量好MnO2慢慢加入其中,至反应停止,称量残留物的质量.有关数据如下表所示.求样品中H2O2的质量分数.| 物质 | H2O2溶液样品质量 | MnO2的质量 | 残留物的质量 |
| 质量(g) | 20 | 2.0 | 18.8 |
分析 根据质量守恒定律,烧杯内质量的减少的质量即生成的氧气的质量.根据过氧化氢分解的化学方程式和生成氧气的质量,计算出参与反应的过氧化氢的质量,然后根据质量分数公式计算即可.
解答 解:根据质量守恒定律,反应生成氧气的质量=20g+2.0g-18.8g=3.2g;
设这过氧化氢溶液中溶质过氧化氢的质量为x,
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$O2↑+2H2O
68 32
x 3.2g
$\frac{68}{x}=\frac{32}{3.2g}$
x=6.8g
过氧化氢溶液中溶质质量分数为$\frac{6.8g}{20g}×$100%=34%
答案:样品中H2O2的质量分数为34%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算氧气的质量是正确解答本题的前提和关键.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
4.二甲醚(C2H6O)是一种清洁能源,能替代柴油作车用能源,具有广阔的市场前景.下列有关二甲醚的说法错误的是( )
| A. | 由C、H、O三种元素组成 | B. | 属于有机化合物 | ||
| C. | 相对分子质量为46 | D. | 一个分子中含有3个氢分子 |
2.从微观的角度去分析、解释宏观的现象是化学研究、学习方法之一.下列分析、解释不正确的是( )
| A. | 水蒸发:水分子间距增大,但水分子本身没有发生变化 | |
| B. | 电解水:水分子变成了氧分子和氢分子,但过程中氢、氧原子未发生变化 | |
| C. | 铅和锡熔合得到焊锡:铅原子和锡原子没有发生化合,焊锡是混合物 | |
| D. | 钠氯化合生成食盐:钠原子失1个电子,氯原子得1个电子,元素的种类已变 |
6.关于能源与环境,下列说法正确的是( )
| A. | 核电站是利用化学能来发电的 | |
| B. | 太阳能电池是把太阳能转化为内能的装置 | |
| C. | 天然气是一种清洁能源,人们可以无穷无尽的开采 | |
| D. | 大量的以煤为燃料,是形成酸雨的重要原因 |
4.下列能在无色溶液中能大量共存的一组物质是( )
| A. | K2SO4 Ba(OH)2 KCl | B. | Cu(NO3)2 NaCl KNO3 | ||
| C. | Na2CO3 KNO3 H2SO4 | D. | MgSO4 NaNO3 KCl |
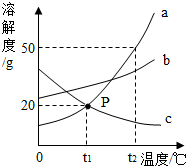 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答: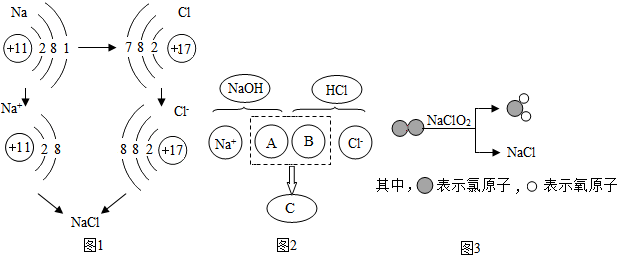
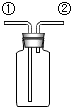 如图是化学中“有名”的装置,有如下用途:
如图是化学中“有名”的装置,有如下用途: