题目内容
锰大量用于制造锰钢.地壳中含锰的矿石有软锰矿,软锰矿的主要成分是二氧化锰.金属锰可用软锰矿跟铝反应来制取,其反应为:3MnO2+4Al
| ||
(1)用100t含MnO2 87%的软锰矿石,理论上可冶炼出
(2)实际冶炼出的锰是含有5%杂质的粗锰,则实际得到
分析:(1)软锰矿石中所含锰元素的质量即是理论上可冶炼出的锰的质量,根据反应的化学方程式,矿石中二氧化锰中锰元素的质量即矿石中锰的质量;
(2)实际冶炼出的锰是含有5%杂质的粗锰,则粗锰中含锰的质量分数为95%,由锰的质量计算所得粗锰的质量.
(2)实际冶炼出的锰是含有5%杂质的粗锰,则粗锰中含锰的质量分数为95%,由锰的质量计算所得粗锰的质量.
解答:解:(1)解法一:100t含MnO2 87%的软锰矿石中二氧化锰的质量为100t×87%=87t
设理论上可冶炼出锰的质量为x
3MnO2+4Al
2Al2O3+3Mn
261 165
87t x
=
x=55t
解法二:根据反应的化学方程式,100t含MnO2 87%的软锰矿石中所含锰元素质量即理论上可冶炼出的锰的质量,
100t含MnO2 87%的软锰矿石中所含锰元素质量=100t×87%×
×100%=55t;
(2)实际冶炼出的锰是含有5%杂质的粗锰,则实际得到粗锰的质量=55t÷(1-5%)≈58t
故答案为:(1)55;(2)58.
设理论上可冶炼出锰的质量为x
3MnO2+4Al
| ||
261 165
87t x
| 261 |
| 87t |
| 165 |
| x |
解法二:根据反应的化学方程式,100t含MnO2 87%的软锰矿石中所含锰元素质量即理论上可冶炼出的锰的质量,
100t含MnO2 87%的软锰矿石中所含锰元素质量=100t×87%×
| 55 |
| 87 |
(2)实际冶炼出的锰是含有5%杂质的粗锰,则实际得到粗锰的质量=55t÷(1-5%)≈58t
故答案为:(1)55;(2)58.
点评:根据化学方程式进行计算时,所使用的质量都是纯净物的质量,混合物的质量不能直接代入化学方程式进行计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 2Al2O3+3Mn
2Al2O3+3Mn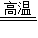 2Al2O3+3Mn
2Al2O3+3Mn