题目内容
18.对比法是重要的研究方法之一,下列探究不需要进行对比实验的是( )| A. | 不同物质的溶解性大小 | B. | 二氧化碳与水是否反应 | ||
| C. | 空气中氧气体积分数的测定 | D. | 物质燃烧的条件 |
分析 利用控制变量法的思想根据对比实验是指只允许一种变量,其它条件相同的实验结合具体实验的原理进行解答.
解答 解:A、比较不同物质的溶解性需要控制溶剂的种类、质量、温度等因素比较溶质溶解的最大限度,所以属于对比实验.
B、利用纸花都是用石蕊溶液染成,都与二氧化碳接触,变量是一瓶内纸花中有水,一瓶内纸花中没有水,由实验可知没有水的纸花没变色,含有水的纸花变成红色,说明二氧化碳与水反应生成了一种酸,酸使石蕊试纸变成红色,所以属于对比实验;
C、研究空气中氧气含量是利用红磷燃烧,消耗空气中氧气,使瓶内气体压强减小,水在外界大气压的作用下进入集气瓶内,所以根本不存在对照实验;
D、铜片上的白磷与铜片上的红磷属于对照实验,都与氧气接触,都属于可燃物,变量是着火点不同,白磷着火点低,红磷着火点高,热水能达到白磷的着火点,达不到红磷的着火点,从而证明可燃物燃烧温度必须达到可燃物的着火点,所以属于对比实验.
故选:C.
点评 解答本题关键是要熟悉对比实验的设计思路,能够分析出变量和不变量,了解通过对比实验能验证出什么结论.

练习册系列答案
相关题目
8.化学的应用就在我们的生产、生活中.下列说法正确的是( )
| A. | 铁丝伸入盛有氧气的集气瓶中,火星四射,生成黑色固体 | |
| B. | 把煤炭粉碎成煤粉,可使煤炭更充分接触空气而燃烧更旺 | |
| C. | 用嘴吹蜡烛,蜡烛熄灭是因为降低了蜡烛的着火点 | |
| D. | 明矾加入水中可净化水,因为明矾有杀菌消毒作用 |
9.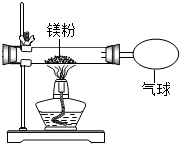 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小红按右图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使无色酚酞试液变色.
做出猜想】黄色固体为Mg3N2
【实验探究】请设计实验,验证猜想
【反思与交流】空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,为什么呢?请给出合理的解释O2比N2化学性质活泼.
 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小红按右图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;
②镁能与氮气反应生成黄色的氮化镁(Mg3N2)固体;
③氮化镁可与水剧烈反应产生氨气,该气体能使无色酚酞试液变色.
做出猜想】黄色固体为Mg3N2
【实验探究】请设计实验,验证猜想
| 实验操作 | 实验现象 | 结论 |
| (1)取样于试管中,加入少量的水 (2)将生成的气体通入到酚酞试液中 | 试管中有气泡产生 溶液呈红色. | 黄色固体为Mg3N2 |

