��Ŀ����
��������������벻��������
��1�������Ƴ��������������ý������������õ� ��
��2��ij�ͺ����Ͻ��к��������軯þ��Mg2Si�������й�Ԫ�صĻ��ϼ�Ϊ ��
��3��ijͬѧ��������˿�ֱ���������ͭ��Һ����������Һ�У��۲쵽������˿�Ͼ��й��帽�ţ��ɴ˵ó��Ľ�����Թ�ϵ�� ��
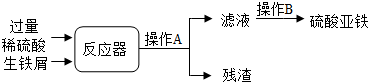
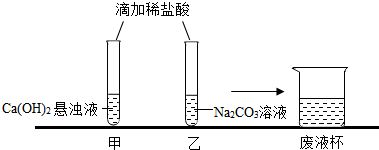
��4����ͼ�����ò������������м�����������������̣�
��ʵ��������ɲ���Aʹ�õIJ��������в��������ձ��� ��
���ڷ�Ӧ���з�����Ӧ�Ļ�ѧ����ʽ��Fe2��SO4��3+Fe=3FeSO4�⣬���� ��
����Һ�п϶����е������� ��

��1�������Ƴ��������������ý������������õ�
��2��ij�ͺ����Ͻ��к��������軯þ��Mg2Si�������й�Ԫ�صĻ��ϼ�Ϊ
��3��ijͬѧ��������˿�ֱ���������ͭ��Һ����������Һ�У��۲쵽������˿�Ͼ��й��帽�ţ��ɴ˵ó��Ľ�����Թ�ϵ��
��4����ͼ�����ò������������м�����������������̣�
��ʵ��������ɲ���Aʹ�õIJ��������в��������ձ���
���ڷ�Ӧ���з�����Ӧ�Ļ�ѧ����ʽ��Fe2��SO4��3+Fe=3FeSO4�⣬����
����Һ�п϶����е�������
���㣺�������������ʼ���;,���˵�ԭ������������Ӧ��,�����Ļ�ѧ����,�������˳����Ӧ��,�й�Ԫ�ػ��ϼ۵ļ���
ר�⣺�������������
��������1�������������õ���չ�ԡ����硢���ȵ����ܣ�
��2���ݻ��������������ϼ۵Ĵ�����Ϊ�������
��3�����ݽ����εķ�Ӧ���ɣ�����ʵ�����۲쵽���������жϽ������ǿ����ϵ���ɣ�
��4���ٹ��˲����еIJ��������в��������ձ���©��
�ھ��������������Ӧ�Ļ�ѧ��Ӧ��
�۸��ݻ�ѧ��Ӧȷ����Һ�е����ʣ�
��2���ݻ��������������ϼ۵Ĵ�����Ϊ�������
��3�����ݽ����εķ�Ӧ���ɣ�����ʵ�����۲쵽���������жϽ������ǿ����ϵ���ɣ�
��4���ٹ��˲����еIJ��������в��������ձ���©��
�ھ��������������Ӧ�Ļ�ѧ��Ӧ��
�۸��ݻ�ѧ��Ӧȷ����Һ�е����ʣ�
����⣨1�������Ƴ��������������ý������������õ���չ�ԣ�
��2����Mg2Si����֪þԪ�صĻ��ϼ�Ϊ+2�ۣ����Ļ��ϼ�Ϊx����+2����2+x=0 ��x=-4�����й�Ԫ�صĻ��ϼ�Ϊ-4��
��3����ʵ��֪����������ͭ��Ӧ˵��Fe��Cu����������������Ӧ�������û�������˵�� Fe��Ag��
��4������ͼ������A����Ϊ���ˣ����˹�����ʹ�õIJ��������в��������ձ���©��
���ڷ�Ӧ���з�����Ӧ�Ļ�ѧ����ʽ��Fe2��SO4��3+Fe=3FeSO4�⣬���� Fe+H2SO4=FeSO4+H2�� Fe2O3+3 H2SO4=Fe2��SO4��3+3 H2O��
����ͼ֪�������������������һ��������Ӧ������������������Һ�п϶����е������� FeSO4��H2SO4��
�ʴ�Ϊ����1����չ�� ��2��-4
��3���������˳��ΪFe��Cu Fe��Ag
��4����©��
��Fe+H2SO4 FeSO4+H2�� Fe2O3+3 H2SO4 Fe2��SO4��3+3 H2O��ÿ������ʽ1�֣�
��FeSO4��H2SO4
��2����Mg2Si����֪þԪ�صĻ��ϼ�Ϊ+2�ۣ����Ļ��ϼ�Ϊx����+2����2+x=0 ��x=-4�����й�Ԫ�صĻ��ϼ�Ϊ-4��
��3����ʵ��֪����������ͭ��Ӧ˵��Fe��Cu����������������Ӧ�������û�������˵�� Fe��Ag��
��4������ͼ������A����Ϊ���ˣ����˹�����ʹ�õIJ��������в��������ձ���©��
���ڷ�Ӧ���з�����Ӧ�Ļ�ѧ����ʽ��Fe2��SO4��3+Fe=3FeSO4�⣬���� Fe+H2SO4=FeSO4+H2�� Fe2O3+3 H2SO4=Fe2��SO4��3+3 H2O��
����ͼ֪�������������������һ��������Ӧ������������������Һ�п϶����е������� FeSO4��H2SO4��
�ʴ�Ϊ����1����չ�� ��2��-4
��3���������˳��ΪFe��Cu Fe��Ag
��4����©��
��Fe+H2SO4 FeSO4+H2�� Fe2O3+3 H2SO4 Fe2��SO4��3+3 H2O��ÿ������ʽ1�֣�
��FeSO4��H2SO4
�����������ѶȲ��Ǻܴ����ս������˳����Ӧ�ò���������ý��з������⡢�����������ȷ�����Ĺؼ���

��ϰ��ϵ�д�
�����Ŀ
����װ����ʾ��ʵ���У��ܴﵽʵ��Ŀ���ǣ�������
A�� ��ȡ0.3mLˮ |
B�� ��˫��ˮ�Ͷ������������� |
C�� ���װ�������� |
D�� ��ȥ�����е�ˮ���� |
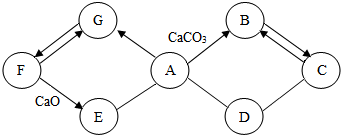
 ��ͼ��ʾ��A��B��C��D��E��F���dz��л�ѧ�������ʣ�A��B�������Ǹ��ֽⷴӦ��B��C���������кͷ�Ӧ������D��ʹ����ʯ��ˮ����ǣ�F������������ˮ������ʳƷ���Σ����ͼ����Ϣ���ش��й����⣺
��ͼ��ʾ��A��B��C��D��E��F���dz��л�ѧ�������ʣ�A��B�������Ǹ��ֽⷴӦ��B��C���������кͷ�Ӧ������D��ʹ����ʯ��ˮ����ǣ�F������������ˮ������ʳƷ���Σ����ͼ����Ϣ���ش��й����⣺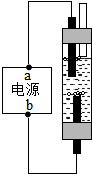 ˮ��һ����������������ģ�����Ӧ���˽��й�ˮ��һЩ֪ʶ��
ˮ��һ����������������ģ�����Ӧ���˽��й�ˮ��һЩ֪ʶ��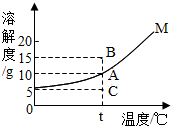 ��ͼ�ǹ�������M��ˮ�е��ܽ�����ߣ���֪A��B��C���������ֱ�ΪA��t��10����B��t��15����C��t��5������ش������й����⣺
��ͼ�ǹ�������M��ˮ�е��ܽ�����ߣ���֪A��B��C���������ֱ�ΪA��t��10����B��t��15����C��t��5������ش������й����⣺
 a��b��c�������ʵ��ܽ��������ͼ��ʾ��
a��b��c�������ʵ��ܽ��������ͼ��ʾ��